
| A. | 共生成0.1mol氧化钙 | |
| B. | 煅烧越充分则消耗的盐酸越少 | |
| C. | 共生成0.1mol二氧化碳 | |
| D. | 煅烧后固体中氧元素的质量分数减小 |
分析 A.根据10g碳酸钙的物质的量是0.1mol,结合钙元素守恒,生成的氧化钙也是0.1mol进行分析;
B.根据碳酸钙、氧化钙和盐酸都会生成氯化钙,然后结合钙元素守恒进行解答;
C.根据碳酸钙高温生成氧化钙和二氧化碳进行分析;
D.根据反应前固体是碳酸钙,反应后的固体是氧化钙进行分析.
解答 解:10g碳酸钙的物质的量为:$\frac{10g}{100g/mol}$=0.1mol,
A.10g碳酸钙的物质的量是0.1mol,结合钙元素守恒,生成的氧化钙也是0.1mol,故A正确;
B.碳酸钙、氧化钙和盐酸都会生成氯化钙,然后结合钙元素守恒可知,最终生成的氯化钙始终是0.1mol,所以消耗的盐酸与碳酸钙的分解程度无关,故B错误;
C.根据反应CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2可知,0.1mol碳酸钙完全分解生成0.1mol二氧化碳,故C正确;
D.反应前固体是碳酸钙,反应后的固体是氧化钙,所以煅烧后固体中氧元素的质量分数减小,故D正确;
故选B.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题有利于提高学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②③ | D. | 没有 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{53}^{131}$I放出射线是一个自发的化学变化过程,射线对人危害很大 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | H2和T2是两种不同的物质,互称为同位素 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 2.0 mol/L的醋酸溶液中氢离子为0.2 NA | |
| B. | 标准状况下,11.2L乙醇所含分子数为0.5NA | |
| C. | 71gCl2与足量的氢氧化钠反应,转移的电子数为2NA | |
| D. | 常温常压下,32gO2和O3的混合气体含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=v(NH3) | C. | 2v(N2)=v(NH3) | D. | v(N2)=3v(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠的水解:CO32-+2H2O?H2CO3+2OH- | |
| B. | 钠和CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ | |
| C. | 用食醋溶解水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
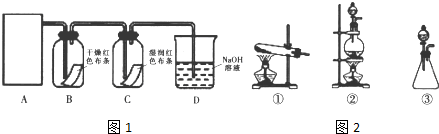
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com