
某有机物在氧气中充分燃烧,生成的水蒸气和二氧化碳的物质的量之比为1∶1,由此可以得出的结论是
( )
A.该有机物中C、H、O的原子个数比为1∶2∶3
B.分子中C、H的原子个数比为1∶2
C.有机物中必定含氧
D.有机物中必定不含氧
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数,下列说法正确的是( )
A.0.2 mol H2O2完全分解转移的电子数为0.4NA
B.含NA个Na+的Na2O溶于1L水中,Na+的物质的量浓度为1mol·L-1
C.在标准状况下,2.8g N2和2.24LCO所含电子数均为1.4NA
D. 2.24L SO2与O2混合气体中所含氧原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)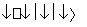 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
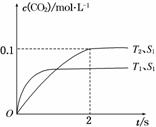
据此判断:
①该反应的ΔH________0(填“>”或“<”)
②在T2温度下,0~2 s内的平均反应速率v(N2)=______________________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。
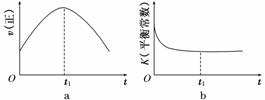
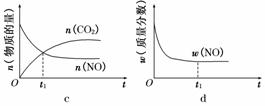
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产 生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g)N2O4(g) ΔH2=-56 .9 kJ/mol
.9 kJ/mol
写出CH4(g)催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式:________________________________________________________________________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的
目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为__________________________。
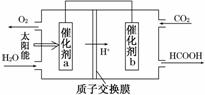
③常温下,0.1 mol·L-1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,在等体积的①pH=0的H2SO4溶液、②0.05 mol/L的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
A.1∶10∶1010∶109 B.1∶5∶5×109∶5×108
C.1∶20∶1010∶109 D.1∶10∶104∶109
查看答案和解析>>
科目:高中化学 来源: 题型:
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、0.1 mol·L-1NH4Cl溶液、NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?________(填“是”或“否”)并说明理由_______________________
________________________________________________________________________。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH为b,若要确认NH3·H2O是弱电解质,则a、b值应满足什么关系?________(用“等式”或“不等式”表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变浅。你认为这一方法能否证明NH3·H2O是弱电解质?并说明原因:
________________________________________________________________________
________________________________________________________________________。
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明 NH3·H2O是弱电解质:
NH3·H2O是弱电解质:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是
( )
A.蒸馏常用于分离提纯液态有机混合物
B.燃烧法是研究确定有机物成分的有效方法
C.核磁共振氢谱通常用于分析有机物的相对分子质量
D.对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组在查阅资料时发现:
实验室制备苯甲醇和苯甲酸的化学原理是:
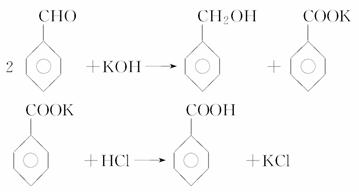
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃,苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
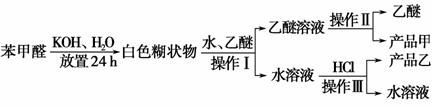
试根据上述信息回答下列问题:
(1)操作Ⅰ的名称是________,乙醚溶液中所溶解的主要成分是________。
(2)操作Ⅱ的名称是________,产品甲是________。
(3)操作Ⅲ的名称是________,产品乙是________。
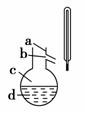 (4)如右图所示,操作Ⅱ中温度计水银球上沿放置的位置应是________(填“a”、“b”、“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是________________,收集产品甲的适宜温度为________。
(4)如右图所示,操作Ⅱ中温度计水银球上沿放置的位置应是________(填“a”、“b”、“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是________________,收集产品甲的适宜温度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是________。
A.冷水 B.沸水
C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学方程式:____________________________。
(3)怎样用最简捷的方法检验制得的物质是胶体?__________________________ _________________________________________________________________________。
(4)取少量制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是____________________,这种现象称为胶体的______________________。
(5)氢氧化铁胶体稳定存在的主要原因是________。
A.胶体微粒直径小于1 nm B.胶体微粒带正电荷
C.胶体微粒做布朗运动 D.胶体微粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液的最本质特征是________。
A.Fe(OH)3胶体微粒的直径在1~100 nm之间
B.Fe(OH)3胶体具有丁达尔现象
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作及现象能够达到对碰实验目的的是
| 选项 | 实验操作及现象 | 实验目的 |
| A | 溶液中滴加盐酸酸化氯化钡溶液出现白色沉淀 | 检验溶液中存在SO42- |
| B | FeBr2溶液加入少量氯水,溶液有浅绿色变为黄色 | 比较Fe2+、Br-还原性强弱 |
| C | 向一定浓度Na2SiO3溶液中通CO2,溶液变浑浊 | 比较C 、Si非金属性强弱 |
| D | 将气体通入饱和碳酸钠溶液的洗气瓶 | 除去中CO2的SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com