
【题目】设NA为阿伏加徳罗常数的值,下列说法不正确的是( )
A. 9.2g NO2和N2O4的混合物中含氮原子数目为0.2NA
B. 常温常压下,35.5g Cl2与足量的NaOH溶液完全反应,转移的电子数为0.5NA
C. 标准状况下,2.24LNH3与1.6gCH4分子中所含电子数目均为NA
D. 已知反应N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4kJ mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ
2NH3(g)△H=-92.4kJ mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】【2017届株洲市上学期教学质检】甲、乙、丙、X是中学化学中常见的4种物质,其转化关系如图,其中甲和X不可能是
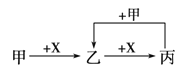
A.甲为C2H5OH、X为O2 B.甲为H2S、X为O2
C.甲为HNO3 、X为Fe D.甲为AlCl 3 溶液、X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
纯净物 | 碱性氧化物 | 酸性氧化物 | 强电解质 | |
① | 漂白粉 | SiO2 | CO2 | AlCl3溶液 |
② | CuSO45H2O | Na2O2 | N2O5 | NH4NO3 |
③ | 福尔马林 | CaO | Mn2O7 | HClO |
④ | 冰醋酸 | Na2O | SO2 | HCl |
A. ① B. ② C. ③ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中,错误的是
A.制钠:以海水为原料制得NaCl,再电解熔融NaCl得钠
B.制铁:以焦炭和铁矿石为原料,用CO还原铁矿石得铁
C.制硅:用焦炭还原二氧化硅得硅
D.制镁:以海水为原料,经一系列过程制得氯化镁,用H2还原MgCl2得镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中,有关试剂的保存方法不正确的是
A. 少量碳酸钙固体放在广口瓶中 B. 新制氯水保存在无色细口瓶中
C. 少量金属钠保存在煤油中 D. 浓硝酸保存在棕色细口瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2+是一种非常好的还原剂,能够与很多氧化剂发生反应。
(1)在加热条件下,FeSO4可与硫酸酸化的KNO3反应,其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NO气体。
①请写出该化学反应方程式,并用单线桥表示出电子转移的方向和数目_________________。
②上述反应发生还原反应的物质是______________ 。
③若11.4gFeSO4参与反应,则产生NO气体的体积(标况下)___________L。
(2)难溶物FeS能够与硫酸酸化的KMnO4溶液反应,反应方程式如下:
10FeS+6KMnO4+24H2SO4=3K2SO4+6MnSO4+5Fe2(SO4)3+l0 +24H2O
①横线上的物质的化学式是___________。
②该反应的氧化产物是______________。
③若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生转移的电子数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能量的变化及反应热的说法中正确的是
A.任何化学反应都有反应热
B.某些化学键断裂时吸收能量,某些化学键断裂时放出能量
C.形成新化学键不一定放出能量
D.有热量变化的过程一定有化学键的断裂与形成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com