
【题目】除去苯中少量苯酚的方法是( )
A.加氯化铁溶液,分液B.加浓溴水,过滤
C.加液溴,反应后蒸馏D.加氢氧化钠溶液,分液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】多原子分子中各原子若在同一平面,且有2个以上相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,下列物质中存在“离域π键”的是( )
A.SO2B.PO43-C.H2SD.HCHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题列举的四个选项是4位同学在学习“化学反应速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是:
A. 化学反应速率理论是研究怎样在一定时间内快出产品
B. 化学平衡理论是研究怎样使用有限原料多出产品
C. 化学反应速率理论是研究怎样提高原料转化率
D. 化学平衡理论是研究怎样使原料尽可能多地转化为产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组通过实验探究NO能否与Na2O2反应以及反应后的产物,该活动小组同学设计了如图所示装置(夹持仪器、连接用的乳胶管均已省略)。
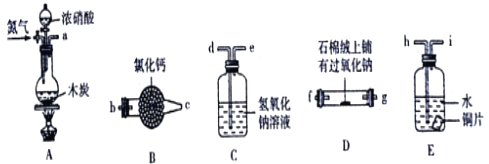
经査阅资料知:①NO是不成盐氧化物;②2NO2+2NaOH =NaNO3+NaNO2+H2O。
回答下列问题:
(1)写出木炭与浓硝酸反应的化学方程式:__________________________________。
(2)为了完成实验,同学甲选择上图中的装置,其连接顺序为a→h→i→d→e→b→c→f;但有同学乙认为该装置存在两处缺陷,则该缺陷是______________、______________。
(3)按改进后的方案连接,检验装置的气密性,装入药品后,要通入一段时间的氮气,再滴入浓硝酸,点燃酒精灯,通入氮气的主要目的是_________________________________。
(4)如果将连接顺序h→i→d→e改为d→e→h→i,会产生怎样的后果,请简述__________________________________________________________________。
(5)已知NO与Na2O2反应的产物为NaNO3和NaNO2的混合物,为了测定产物中NaNO2含量,该小组同学准确称取反应后的固体3.50g,用煮沸并冷却后的蒸馏水配成100.00mL溶液,取10.00mL溶液于锥形瓶中,用0.1000mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液20mL。滴定过程中发生反应的离子方程式为_______________________,反应产物中NaNO2的质量分数为___________(保留四位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3 kJ·mol1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol1
B. 甲烷的标准燃烧热ΔH=-890.3 kJ·mol1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol1
C. 已知:500℃、30MPa下,N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D. CO(g)的燃烧热是283.0kJ·mol1,则2CO2(g) ===2CO(g)+O2(g)反应的△H=+566.0 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应“P4(s)+3NaOH(aq)+3H2O(l)=3NaH2PO2(aq)+PH3(g) ΔH>0”制得的NaH2PO2可用于化学镀镍。下列说法正确的是

A. P4分子中P原子均满足8电子稳定结构
B. 反应中NaOH作还原剂
C. 该反应能自发进行,则ΔS<0
D. 反应中生成1 mol NaH2PO2,转移电子数目为3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂冶炼钛精矿得到钛渣,钛渣的成分及含量(质量分数)为:TiO251.00%、Al2O319.34%、MgO7.20%、CaO4.00%、SiO218.46%,通过下列工艺流程可以得到纳米二氧化钛和某型分子筛(化学式为Na4Al4Si4O16 9H2O)。
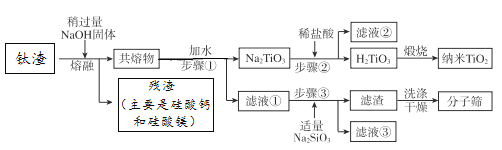
下列说法不正确的是
A. 钛渣中的TiO2、SiO2不属于碱性氧化物
B. 滤液①中溶质只有NaAlO2、NaOH
C. 步骤②中加入盐酸时,反应的离子方程式是Na2TiO3 + 2H+![]() H2TiO3↓+2Na+
H2TiO3↓+2Na+
D. 步骤③中加入适量Na2SiO3时,反应的化学方程式为:4NaAlO2 + 4Na2SiO3 +13H2O ![]() Na4Al4Si4O16 9H2O↓ + 8NaOH
Na4Al4Si4O16 9H2O↓ + 8NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图Ⅰ所示,若其他条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是( )
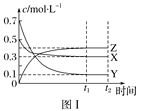
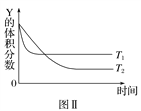
A. 该反应的热化学方程式为X(g)+3Y(g) ![]() 2Z(g) ΔH>0
2Z(g) ΔH>0
B. 若其他条件不变,升高温度,正、逆反应速率均增大,X的转化率增大
C. 温度分别为T1和T2时的平衡常数大小关系为K2>K1
D. 达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com