
【题目】将13.6gCu和Cu2O组成的混合物加入250 mL—定浓度的稀硝酸中,固体完全溶解生成Cu(NO3)2和NO。向所得溶液中加入1.0 L 0.5 mol L-1的NaOH溶液,生成沉淀的质量为19.6 g,此时溶液呈中性,且金属离子(钠离子除外)沉淀完全。下列说法正确的是
A. 原固体混合物中,Cu和Cu2O的物质的量之比为1:1
B. 原稀硝酸的浓度为1.3 mol·L-1
C. 固体溶解后剩余硝酸的物质的量为0.1 mol
D. 产生的NO的体积为2.24L
【答案】C
【解析】
向所得溶液中加入0.5mol/L 的NaOH溶液1L,溶液呈中性,金属离子已完全沉淀,此时溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=0.5mol/L×1L=0.5ml,沉淀为Cu(OH)2,质量为19.6g,其物质的量为:![]() =0.2mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.2mol,
=0.2mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.2mol,
A.设Cu和Cu2O的物质的量分别为xmol、ymol,根据二者质量有 64x+144y=13.6,根据铜元素守恒有x+2y=0.2,联立方程解得x=0.1,y=0.05,则:n(Cu):n(Cu2O)=0.1mol:0.05mol=2:1,故A错误;
B.根据选项N元素守恒可知n(HNO3)=n(NO)+n(NaNO3),根据电子转移守恒可知:3n(NO)=2n(Cu)+2n(Cu2O),所以3n(NO)=2×0.1mol+2×0.05mol,解得n(NO)=0.1mol,根据Na元素可知n(NaNO3)=n(NaOH)=0.5mol/L×1L=0.5mol,所以n(HNO3)=n(NO)+n(NaNO3)=0.1mol+0.5mol=0.6mol,所以原硝酸溶液的浓度为:![]() =2.4mol/L,选项B错误;
=2.4mol/L,选项B错误;
C.反应后的溶液中加入氢氧化钠溶液,部分氢氧化钠与硝酸铜反应,部分氢氧化钠与硝酸反应,最后为硝酸钠溶液,根据氮元素守恒可知反应后溶液中n(HNO3)+2n[[Cu(NO3)2]=n(NaNO3),所以n(HNO3)=n(NaNO3)-2n[[Cu(NO3)2]=0.5mol-2×0.2mol=0.1mol,选项C正确;
D.由B中计算可知n(NO)=0.1mol,所以标准状况下NO的体积为:0.1mol×22.4L/mol=2.24L,选项D错误;
答案选C。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO |
B | 向稀氨水和酚酞混合溶液中加入少量Ag2O,振荡 | 溶液由浅红色变为红色 | Ag2O是强碱 |
C | 向装有经过硫酸处理的CrO3(桔红色)的硅胶导管中吹入乙醇蒸气 | 固体逐渐由桔红色变为浅绿色(Cr3+) | 乙醇具有还原性 |
D | 向盛有少量水的烧杯中加入少量Mg2Si | 产生白色沉淀,液面上有火苗 | Mg2Si水解生成Mg(OH)2和SiH4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】艾司洛尔是预防和治疗手术期心动过速或高血压的一种药物,艾司洛尔的一种合成路线如下:
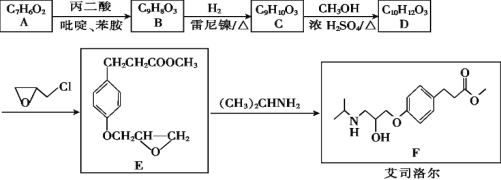
回答下列问题:
(1)丙二酸的结构简式为_______;E中含氧官能团的名称是_______。
(2)D生成E的反应类型为____________。
(3)C的结构简式为________________。
(4)A遇FeCl3溶液发生显色反应,1 mol A和1 mol丙二酸在吡啶、苯胺中反应生成1 mol B、1 mol H2O和1 mol CO2,B能与溴水发生加成反应,推测A生成B的化学方程式为____。
(5)X是B的同分异构体,X同时满足下列条件的结构共有____种,其中核磁共振氢谱有五组峰的结构简式为____。
①可与碳酸氢钠溶液反应生成二氧化碳
②遇FeCl3溶液发生显色反应
③除苯环外不含其他环
(6)写出以苯甲醇和丙二酸为原料制备![]() 的合成路线________(其他试剂任选)。
的合成路线________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
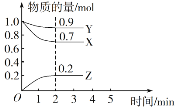
(1)该反应的化学方程式为_______________。
(2)反应开始至2 min,以气体Z表示的平均反应速率为________。
(3)可以判断上述反应已经达到平衡的是________。
A.v(A)∶v (B)∶v (C)等于化学计量数之比
B.密闭容器中总压强不变 C.密闭容器中混合气体的密度不变
D.混合气体的平均相对分子质量不再改变 E.n(A)∶n(B)∶n(C)等于化学计量数之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图所示转化关系(X代表卤素),说法不正确的是

A.2H(g) +2X(g) == 2HX(g) ΔH3<0
B.途径Ⅰ生成HX的反应热与途径无关,所以ΔH1 = ΔH2 + ΔH3
C.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多
D.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是 ( )

A. ③中选用NaOH溶液吸收多余的SO2
B. 上下移动①中铜丝可控制SO2的量
C. ②中选用品红溶液验证SO2的生成
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)之后才能排放。
(1)在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①2CO(g)+O2(g) ![]() 2CO2(g) ΔH=566.0 kJ·mol1
2CO2(g) ΔH=566.0 kJ·mol1
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+180.0 kJ·mol1
2NO(g) ΔH=+180.0 kJ·mol1
③2NO(g)+O2(g) ![]() 2NO2(g) ΔH=116.5 kJ·mol1
2NO2(g) ΔH=116.5 kJ·mol1
回答下列问题:
①CO的燃烧热ΔH为 _________。若1 mol N2(g)、1 mol O2(g) 分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g) 分子中化学键断裂时需吸收的能量为_________kJ。
②CO将NO2还原为单质的热化学方程式为 ________________。
(2)图是一种用NH3脱除烟气中NO的原理。
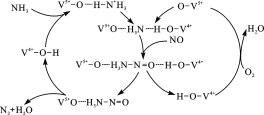
①该原理中,NO最终转化为H2O和_______(填化学式)。
②当消耗1 mol NH3和0.5 mol O2时,除去的NO在标准状况下的体积为____L。
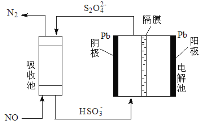
(3)间接电化学法,如图所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式_____________。用离子方程式表示吸收池中除去NO的原理_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%,质量分数),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO47H2O的工艺流程如下:
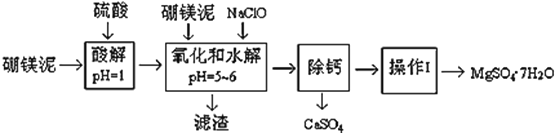
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,量取浓硫酸需要使用量筒的规格为__________(填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl ,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有__________,___________。
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法___________________。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤______。“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,______,便得到了MgSO47H2O
(6)实验中提供的硼镁泥共100 g,得到 MgSO47H2O为172.2 g ,则MgSO47H2O 的产率为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com