
下列关于化学反应限度的说法中正确的是()
A. 平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
B. 化学反应的限度不可以通过改变条件而改变
C. 当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度
D. 当一个可逆反应达到平衡状态时,那么这个反应的正反应速率和逆反应速率为零
考点: 化学平衡建立的过程;化学平衡的影响因素.
分析: 在不同的条件下,化学反应限度不同,当达到化学反应限度时,正逆反应速率相等但不为0,反应物的浓度和生成物的浓度不再改变,当外界条件发生改变,平衡发生移动,化学反应限度变化.
解答: 解:A.化学平衡状态随外界条件的改变而改变,为动态平衡,不是静止的状态,故A错误;
B.当外界条件发生改变,平衡发生移动,化学反应限度变化,故B错误;
C.在一定条件下,当正逆反应速率相等时,可逆反应达到一定的限度,即平衡状态,故C正确;
D.当反应达到化学平衡状态时,正逆反应速率相等但不为0,故D错误;
故选C.
点评: 本题考查化学反应平衡状态的判断,题目难度不大,本题注意理解化学反应限度与化学平衡状态的特征和判断角度.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
【实验一】用如图CB31所示装置,收集一量筒甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
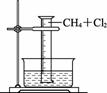
图CB31
(1)该反应的反应类型为______________。
(2)该反应的化学方程式为____________________________________________________
(只写第一步)。
(3)水槽中盛放的液体应为________(填标号)。
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
【实验二】收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(4)该实验设计的错误之处是_________________________________________________。
【实验三】步骤一:收集半试管氯气,加入10 mL蒸馏水,充分振荡,采用DIS系统的pH传感器测量溶液的pH(下同),测得pH=3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL蒸馏水,充分振荡,测得pH=1.00。
(5)判断该反应中有氯化氢生成的依据是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第ⅠB族。Cu2+的核外电子排布式为 。
(2)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知
NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原
因是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
表明金属甲比金属乙活动性强的叙述正确的是()
A. 在氧化还原反应中,甲失的电子比乙多
B. 同价态阳离子,甲比乙氧化性强
C. 将甲和乙用导线相连接,一同放入CuSO4溶液中,乙的表面有红色的铜析出
D. 将甲、乙组成原电池时,甲为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于ⅦA族元素的叙述正确的是()
A. ⅦA族元素是同周期中原子半径最大的元素
B. ⅦA族元素其简单阴离子的核外电子层数等于该元素所在的周期数
C. ⅦA族元素的最高正价都是+7价
D. ⅦA族元素是同周期中非金属性最弱的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4A(g)+5B(g)⇌4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是()
A. 30min中A的平均反应速率是0.010mol•L﹣1•min﹣1
B. 容器中D的物质的量一定增加了0.45mol
C. 容器中A、B、C、D的物质的量的比一定是4:5:4:6
D. 容器中A的物质的量一定增加0.30mol
查看答案和解析>>
科目:高中化学 来源: 题型:
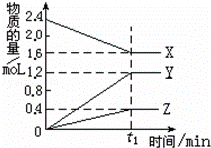
某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
(1)①该反应的化学方程式.
②在t1min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为2:3
C.生成3mol Y的同时生成1mol Z
D.生成1mol Z的同时生成2mol X
(2)①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1min时,该反应吸收的热量为:;在此t1min时间内,用H2表示反应的平均速率v(H2)=.
②两位同学讨论放热反应和吸热反应.甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应.你认为他们说法正确的是同学.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组混合物中,都能用分液漏斗的是( )
|
| A. | 乙酸乙酯和水 酒精和水 苯酚和水 |
|
| B. | 溴乙烷和水 溴苯和水 硝基苯和水 |
|
| C. | 甘油和水 己烷和水 甲酸和水 |
|
| D. | 苯和甲苯 乙醛和水 乙酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分子式为C12H12的物质A的结构简式为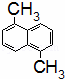 ,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
A. 9种 B. 10种 C. 11种 D. 12种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com