
����Ŀ��10 ������NaHCO3������Һ����ø���Һ��pH�������µı仯��
�¶�(��) | 10 | 20 | 30 | ������к���ȴ��50 �� |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)��ͬѧ��Ϊ������Һ��pH���ߵ�ԭ����HCO3-��ˮ��̶����ʼ�����ǿ����ˮ�ⷴӦ�����ӷ���ʽΪ______________��
(2)��ͬѧ��Ϊ����ҺpH���ߵ�ԭ����NaHCO3���ȷֽ⣬������Na2CO3�����ƶ�Na2CO3��ˮ��̶�________(��������������С����)NaHCO3���÷ֽⷴӦ�Ļ�ѧ����ʽΪ____��
(3)��ͬѧ��Ϊ�ס��ҵ��ж϶�����֡�����Ϊ��
��ֻҪ�ڼ�����е���Һ�м����������Լ�BaCl2��Һ�������������������ж���ȷ��ԭ����____________��д����Ӧ�����ӷ���ʽ�����ܲ���ѡ��Ba(OH)2��Һ��______(������������������)��
�������Ⱥ����Һ��ȴ��10 ��������Һ��pH________(������������С��������������)8.3����________(����������������)�ж���ȷ��
���𰸡�HCO3-��H2OH2CO3��OH�� ���� 2NaHCO3![]() Na2CO3��CO2����H2O Ba2����CO32-=BaCO3�� ���� ���� ��
Na2CO3��CO2����H2O Ba2����CO32-=BaCO3�� ���� ���� ��
��������
��1��NaHCO3Ϊǿ�������Σ�����Һ�з�����HCO3-+H2OH2CO3+OH-��ˮ��ʼ��ԣ�
�ʴ�Ϊ��HCO3-+H2OH2CO3+OH-��
��2������ʱ��NaHCO3�ɷֽ�����Na2CO3����Ӧ�Ļ�ѧ����ʽΪ2NaHCO3![]() Na2CO3��CO2����H2O��̼���һ��������ڶ������룬Na2CO3ˮ��̶ȴ���NaHCO3��ˮ��̶ȣ���Һ���Խ�ǿ��
Na2CO3��CO2����H2O��̼���һ��������ڶ������룬Na2CO3ˮ��̶ȴ���NaHCO3��ˮ��̶ȣ���Һ���Խ�ǿ��
�ʴ�Ϊ�����ڣ�2NaHCO3![]() Na2CO3��CO2����H2O
Na2CO3��CO2����H2O
��3���ټ����Ȼ�����Һ�������ɳ�����˵����Һ�д���CO32-����Ӧ�����ӷ���ʽΪBa2++CO32-=BaCO3������ͬѧ������ȷ��ѡ��Ba��OH��2��Һ��̼�����ơ�̼���ƶ��ᷴӦ�������ɰ�ɫ���������Բ���ѡ����������Һ��
�ʴ�Ϊ�� Ba2++CO32-=BaCO3�������ܣ�
���ɱ�����ҺpH������֪�������Ⱥ����Һ��ȴ��10�棬����Һ��pH����8.3��˵��̼������û�зֽ⣬�����ȷ��
�ʴ�Ϊ�����ڣ��ס�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L�ܱ������г���4molA�����3molB���壬�������з�Ӧ��2A(g)+B(g) ![]() C(g)+xD(g)��5s�ﵽƽ�⡣�ﵽƽ��ʱ��������1mol C���ⶨD��Ũ��Ϊ1mol/L��
C(g)+xD(g)��5s�ﵽƽ�⡣�ﵽƽ��ʱ��������1mol C���ⶨD��Ũ��Ϊ1mol/L��
(1)��x =____��
(2)�����ʱ��A��ƽ����Ӧ����Ϊ_____��
(3)ƽ��ʱB��Ũ��Ϊ______��
(4)����������˵��������Ӧ�ﵽƽ��״̬����_____
A ��λʱ����ÿ����2 mol A��ͬʱ����1molC
B ��λʱ����ÿ����1molB��ͬʱ����1mol C
C D������������ٱ仯
D ��������ѹǿ���ٱ仯
E B��C��Ũ��֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.2mol/L��һԪ��BOH���Ũ�ȵ�HCl��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ������˵����ȷ������ ��

A. BOHΪǿ�� B. �û��ҺpH=7
C. ͼ��X��ʾBOH,Y��ʾH+,Z��ʾOH- D. �û����Һ�У�c(Cl-)=c(Y)+c(B+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ�����һ��ʱ�����Һ�о��а�ɫ�������ɣ����н��۲���ȷ����
ʵ��� | ʵ��� | ʵ��� |
2mL1mol/LBaCl2��Һ 4mL1mol/LNaHCO3��Һ | 2mL1mol/LBaCl2��Һ 4mL1mol/LNa2SO3��Һ | 2mL1mol/LBaCl2��Һ 4mLH2SO3��Һ |
A.ʵ��������ɵij�����BaCO3
B.ʵ���������������
C.ʵ��ڳ����п��ܺ���BaSO4
D.ʵ������ɳ��������ӷ���ʽ�ǣ�Ba2++H2SO3=BaSO3��+2H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɲⶨ�к��ȡ����й��ڸ�ʵ���˵����ȷ����

A.��ʵ��װ�ÿ�����Ͳδ��������ͼ�л�ȱ��һ����Ҫ������
B.����һ���������к��Ȳⶨʵ�飬�¶ȼ���Ҫʹ��2��
C.�ձ������ֽм�������ǹ̶��ձ���λ��
D.����ʵ���������������ɢʧ�����Բ�õ��к��ȡ�H������ֵҪС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼��Ʒ�Ӧ����CO2,������ͼ,�ɲⶨ�÷�Ӧ������.�����Ҫ����գ�

��1�����Ӻ���������Ҫ���_____________________,�ټ���ҩƷ����ʵ��.
��2������ƿ�м���5g����ʯ,����20mL 1mol��L1����.ÿ��10s�۲ⲣ��ע��������������������mL��s1Ϊ��Ӧ���ʵĵ�λ������ÿ10sʱ�����ڵķ�Ӧ���ʡ����ݴ����Ľ��������ı���
ʱ��/s | 10 | 20 | 30 | 40 | 50 | 60 |
�������/mL | 4 | 14 | 25 | 38 | 47 | 55 |
��Ӧ����/mL��s1 | 0.4 | 1.0 | 1.1 | �� | 0.9 | 0.8 |
�����еġ�?����Ӧ���������_________________.
��3���ӷ�Ӧ������ʱ��仯�����ݿ�֪����ʵ���з�Ӧ������___________��__________�й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���Ӧ��6H2(g)+2CO2(g)![]() C2H5OH(g)+3H2O(g)��������ͼ��ʾ��
C2H5OH(g)+3H2O(g)��������ͼ��ʾ��
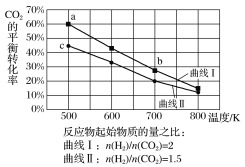
����˵����ȷ���ǣ� ��
A.�÷�ӦΪ���ȷ�Ӧ
B.��ƽ��ʱ��v��(H2)=v��(CO2)
C.b���Ӧ��ƽ�ⳣ��Kֵ����c��
D.a���Ӧ��H2��ƽ��ת����Ϊ90%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����ַdz���Ҫ�Ļ���ԭ�ϣ���ҵ��CO2 ��������ȼ�ϼ״������ܻ�������ЧӦ��ҲΪ�״��ĺϳ�Ѱ������������
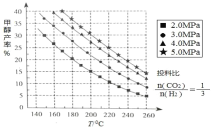
(1)�״��ĺϳɣ��ϳɼ״��ķ�ӦΪ��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H ���ڴ��������£���ü״��IJ����뷴Ӧ�¶ȡ�ѹǿ��ϵ����ͼ��ʾ�� ��ͼ�����ݿ�֪����H______0(ѡ ��������������������)���״���������ѹǿ�仯����ͼʾ���ɵ�ԭ����_______��
(2)�״���Ӧ�ã���Ȳ�������һ����Ҫ���л�����ԭ�ϣ�������ˮ�����³�Һ̬���е�Ϊ 103~105 �档ʵ���ҿ��ü״�����һ�л�ԭ�� M ��һ���������Ʊ���ʵ�鲽�����£�
���� 1���ڷ�Ӧƿ�У����� 13 g ԭ�� M��50 mL �״��� 2 mL Ũ���ᣬ���裬���Ȼ���һ��ʱ�䡣
���� 2�����������ļ״�(װ�ü���ͼ)��
���� 3����ӦҺ��ȴ�������ñ��� NaCl ��Һ�� 5%Na2CO3 ��Һ��ˮϴ�ӣ�������л��ࡣ
���� 4���л��ྭ��ˮ Na2SO4 ������ˡ����� �ñ�Ȳ�������
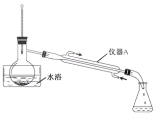
�ٲ��� 1 �з�Ӧ�Ļ�ѧ����ʽ��_____________��
�ڲ��� 1 �У���������״���Ŀ����_____________��
�۲��� 3 �� Na2CO3 ��Һϴ����Ҫȥ����������______���ò����в��õ�����Ũ�ȵ�NaOH ��Һ����Na2CO3 ��Һϴ����Ҫԭ����___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com