
| A.氢氧化钙乳浆 | B.碳酸钠溶液 | C.碳酸氢钠溶液 | D.氢氧化钠溶液 |
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
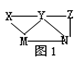
| A.X一定为H2SO4 |
| B.Y一定为K2CO3 |
| C.Z可能为氯水 |
| D.M、N必定各为BaCl2、FeSO4中的一种 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
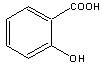 + (CH3CO)2O
+ (CH3CO)2O 
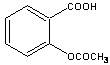 + CH3COOH
+ CH3COOH查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
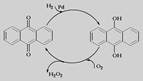
|

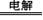 (NH4)2S2O8 + H2↑,
(NH4)2S2O8 + H2↑,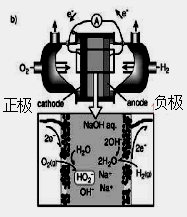
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使硫酸过量 |
| B.使铁屑过量 |
| C.使用稀H2SO4 |
| D.使用浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
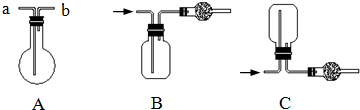
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
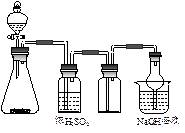
| A.电石和水 |
| B.MnO2和浓盐酸 |
| C.Cu片和浓硝酸 |
| D.Na2SO3和浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com