
在一定条件下,向一体积为2L的恒容密闭容器中充入2mol A,1mol B,发生如下反应: 2A(g)+B  3C(g) △H=-QkJ/mol(Q>0)。经过60s达到平衡,测得B物质的量为0.2mol,下列对该平衡的叙述正确的
3C(g) △H=-QkJ/mol(Q>0)。经过60s达到平衡,测得B物质的量为0.2mol,下列对该平衡的叙述正确的
A.用C的浓度变化表示该反应速率为2.4mol/(L·min)
B.若使容器变为1L,则C的物质的量一定增大
C.达到平衡,测得放出热量为x kJ,则x=Q
D.若向容器再充入1mol C,重新达平衡,A的体积分数保持不变,则B为气态
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:选择题
一定温度下,反应N2(g)+3H2(g)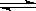 2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g)
2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g)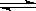 2N2(g)+6H2(g)的反应热和化学平衡常数为
2N2(g)+6H2(g)的反应热和化学平衡常数为
A.2△H和2K B.-2△H和 K2
C.2△H和-2K D.-2△H和 K-2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
下列鉴别方法不可行的是
A.用水鉴别乙醇、甲苯和溴苯
B.用燃烧法鉴别甲烷、乙烯
C.用溴水鉴别直镏汽油、裂化汽油
D.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上期中测试化学试卷(解析版) 题型:实验题
(18分)下图为两套实验装置。
(1)写出下列仪器的名称:

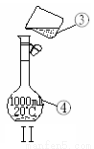
① ;② 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
(3)若利用装置I制取蒸馏水,还缺少的仪器是 ,将仪器补充完整后进行实验,冷却水从 口进。
(4)现需配制1.0 mol·L-1的NaOH溶液240mL,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误分别是 、 。
(5)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为_____________________。
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为_________g,该同学应称量_________g NaOH。
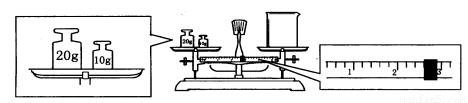
(7)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是__________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上期中测试化学试卷(解析版) 题型:选择题
下列物质分类中,前者包括后者的是
A.金属氧化物 化合物 B.溶液 胶体
C.电解质 化合物 D.混合物 胶体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
B.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
D.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期期中测试化学试卷(解析版) 题型:选择题
在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是
A.n(Cl2)∶n(Fe)=5∶4 5Cl2+4Fe 2FeCl2+2FeCl3
2FeCl2+2FeCl3
B.n(Cl2)∶n(FeBr2)=1∶1 Fe2++2Br-+Cl2=Fe3++Br2+2Cl-
C.n(MnO4-)∶n(H2O2)=2∶3 2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.n(Fe)∶n[HNO3(稀)]=1∶3 4Fe+12H++3NO3-===3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列关系式中,正确的是
A.等浓度等体积的CH3COOH和CH3COONa溶液混合:c(CH3COO- )+c(OH -)=c(H+)+c(CH3COOH)
B.常温下,0.1 mol·L-1 HA溶液与0.1 mol·L NaOH溶液等体积完全反应时,溶液中一定存在:c(Na+)=c(A- )>c(OH )=c(H+)
C.常温下,0.1 mol·L-1 Na2S溶液中存在:c(OH- )=c(H+)+c(HS- )+c(H2S)
D.常温下,将0.1 mol·L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中c(CHCOO-)/c(CHCOOH)的值增大到原来的100倍
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上学期第一次段中考试化学试卷(解析版) 题型:选择题
下列关于电解质溶液中离子浓度关系的说法正确的是
A.0.1mol/L的NaHCO3溶液中离子浓度的关系:c(Na+)=c(HCO3-) + c(H2CO3) + 2c(CO32-)
B.0.1mol/L的NH4Cl溶液和0.1mol/L的NH3·H2O等体积混合后离子浓度的关系:c( Cl-)>c(NH4+)>c(H+)>c (OH-)
C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-)
D.KHS溶液中存在等式关系:2c(S2-) + c(OH-) = c(H+) + c(H2S)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com