
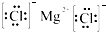 ;(2)NaOH
;(2)NaOH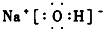 ;(3)HClO
;(3)HClO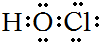 ;(4)H2O2
;(4)H2O2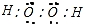 .
. 分析 (1)氯化镁为离子化合物,必须标出阴阳离子的电子式;
(2)氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
(3)HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键;
(4)双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合.
解答 解:(1)氯化镁为离子化合物,化学式中存在阴阳离子,其电子式中需要标出阴阳离子所带电荷,氯化镁的电子式为: ,
,
故答案为: ;
;
(2)NaOH的电子式为: ,故答案为:
,故答案为: ;
;
(3)HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为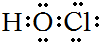 ,故答案为:
,故答案为: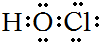 ;
;
(4)双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,故答案为:
,故答案为: .
.
点评 本题考查了电子式的书写,题目难度不大,注意掌握电子式的概念及书写原则,明确离子化合物与共价化合物的电子式表示方法及区别.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | P、Q、R、S的浓度相等 | B. | P、Q、R、S在容器中共存 | ||
| C. | P、Q的反应速率相等内部 | D. | P、Q、R、S的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为2:1 | |
| B. | Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序:R>W>Z | |
| D. | Y分别与Z、W、R以两种元素组成的常见化合物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
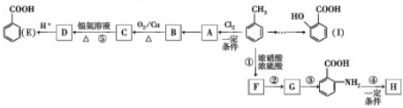
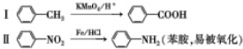
 .
. .写出③的转化关系
.写出③的转化关系 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (用已知中的表达式表示,不用写化学方程式)
(用已知中的表达式表示,不用写化学方程式)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数和质量分别不等 | B. | 质子数相等,质量不等 | ||
| C. | 分子数和质量都相等 | D. | 原子数、中子数和质子数都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 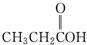 | B. | 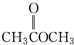 | C. | 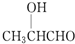 | D. | 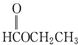 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
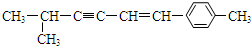 ,关于该有机物的空间构型下列说法中正确的是( )
,关于该有机物的空间构型下列说法中正确的是( )| A. | 该分子中所有的碳原子均可能处于同一平面上 | |
| B. | 该分子中一定共面的碳原子数至少为8个 | |
| C. | 该分子中至少有9个碳原子处于同一条直线上 | |
| D. | 该分子中可能处于同一平面的原子总数最多为16个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
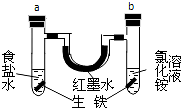 如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )| A. | a中发生了吸氧腐蚀,b中发生了析氢腐蚀 | |
| B. | a中正极反应方程式是:O2+2H2O+4e-═4OH- | |
| C. | a、b试管中生铁块中铁都作电池的负极 | |
| D. | 红墨水在一段时间后,两边液面变为左低右高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 所有金属元素与所有非金属元素间都能形成离子键 | |
| C. | NH4Cl属于离子化合物 | |
| D. | 在离子化合物CaCl2中,两个氯离子间也存在离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com