
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.9 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 9.7 |
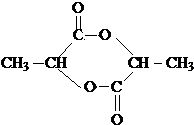 ,聚乳酸的结构简式为
,聚乳酸的结构简式为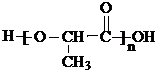 .
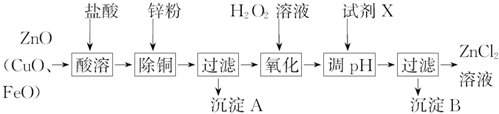
.分析 炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)加盐酸溶解,形成氯化锌、氯化铜、氯化亚铁的溶液,加锌粉置换出Cu,过滤,沉淀A为Cu,滤液中含有锌离子和亚铁离子,加入过氧化氢把亚铁离子氧化为铁离子,再加ZnO(或氢氧化锌等)调节pH,使铁离子转化为氢氧化铁沉淀,过滤除去沉淀,得到氯化锌溶液,
(1)加过氧化氢把亚铁离子氧化为铁离子;
(2)调节pH时要消耗氢离子,但是不能引入杂质;调节pH使铁离子转化为沉淀,而锌离子不沉淀,根据表中数据分析;
(3)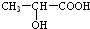 分子中含有-COOH和-OH,结合丙交酯的分子式可知,两分子的乳酸分子间发生酯化反应脱去两分子水生成丙交酯;
分子中含有-COOH和-OH,结合丙交酯的分子式可知,两分子的乳酸分子间发生酯化反应脱去两分子水生成丙交酯;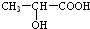 分子间发生缩聚反应生成聚乳酸和水;
分子间发生缩聚反应生成聚乳酸和水;
(4)石墨作电极电解时,阳极氢氧根离子失电子生成氧气与水,阴极上[Zn(OH)4]2-得电子生成Zn与氢氧根离子;
(5)ZnO能溶液强碱溶液,CuO和FeO不溶于碱溶液.
解答 解:(1)根据流程分析可知,加过氧化氢的目的是将亚铁离子氧化为铁离子,
故答案为:将亚铁离子氧化为铁离子;
(2)调节pH时要消耗氢离子,但是不能引入杂质,ZnO、Zn(OH)2、Zn2(OH)2CO3均与氢离子反应生成锌离子,消耗氢离子的同时不引人杂质,ZnSO4不能与氢离子反应,所以不能调节pH,故选abc,调节pH使铁离子转化为沉淀,而锌离子不沉淀,由表中数据可知pH≥3.2时,铁离子完全沉淀,而锌离子开始沉淀的pH为5.2,所以要调节pH为3.2≤pH<5.2;
故答案为:abc;3.2≤pH<5.2;
(3)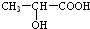 分子中含有-COOH和-OH,两分子的乳酸分子间发生酯化反应,反应产物为
分子中含有-COOH和-OH,两分子的乳酸分子间发生酯化反应,反应产物为 ;
;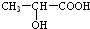 分子间发生缩聚反应生成聚乳酸和水,聚乳酸的结构简式为:
分子间发生缩聚反应生成聚乳酸和水,聚乳酸的结构简式为: ;
;
故答案为: ;
; ;
;
(4)石墨作电极电解时,阳极氢氧根离子失电子生成氧气与水阳极反应为:4OH--4e-═2H2O+O2↑,阴极上[Zn(OH)4]2-得电子生成Zn与氢氧根离子,则阴极的电极方程式为:[Zn(OH)4]2-+2e-=Zn+4OH-,
故答案为:OH-;[Zn(OH)4]2-+2e-=Zn+4 OH-;
(5)ZnO能溶液强碱溶液,CuO和FeO不溶于碱溶液,酸溶液与ZnO、CuO、FeO均能反应,所以炼锌烟尘采用碱溶,而不采用酸溶后电解,
故答案为:氧化铜、氧化亚铁不溶于碱溶液中.
点评 本题考查物质的制备工艺流程,涉及对工艺流程的分析评价、物质的分离提纯、酯化反应和缩聚反应、电解原理的应用等知识点,是对学生综合能力考查,需要学生具备扎实的基础,题目难度中等.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. |  | B. | 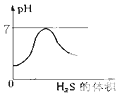 | C. | 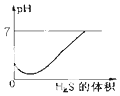 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在原电池的负极和电解池的阳极上发生的都是氧化反应 | |
| B. | 实验室用惰性电极电解NaCl溶液,阴、阳两极收集到的气体体积之比为1:1 | |
| C. | 一定条件下可能发生反应:Cu+H2SO4═CuSO4+H2↑ | |
| D. | 在用惰性电极电解稀硫酸的过程中,溶液pH保持不变. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3作氧化剂 | |
| B. | 氧化剂和还原剂的物质的量之比为1:1 | |
| C. | 当生成1molI2时,转移2mol电子 | |
| D. | 由该反应可知还原性:Se>KI |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
| 相对式量 | 112.5 | 147 | 162.5 | 128 |
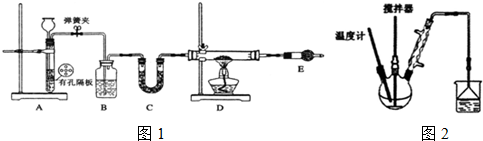
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 伴有能量变化的物质变化,都是化学变化 | |
| B. | 干冰升华时,二氧化碳分子中的共价键不发生断裂 | |
| C. | 凡经加热而发生的化学反应都是吸热反应 | |
| D. | C(石墨,s)═C(金刚石,s),反应中既没有电子得失也没有能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水、次氯酸都属于弱电解质 | |
| B. | 有同种元素组成的物质一定是纯净物 | |
| C. | NaHSO4在溶液中能电离出H+,所以NaHSO4是酸 | |
| D. | 侯氏制碱法法的工艺中应用了物质溶解度的差异 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com