
����Ŀ��A��B��C��D��E��F����Ԫ�ؾ�λ�����ڱ���ǰ�����ڣ���ԭ��������������Ԫ��A��ԭ�Ӱ뾶��С��Ԫ�أ�BԪ�ػ�̬ԭ�ӵĺ�����ӷ�ռ�ĸ�ԭ�ӹ�����ܼ�����DԪ��ԭ�ӵ��ѳɶԵ���������δ�ɶԵ���������3����E��D����ͬһ���壻Fλ��ds������ԭ�ӵ������ֻ��1�����ӣ�
��1��F+���ӵĵ����Ų�ʽ�� ��
��2��B��C��DԪ�صĵ�һ�������ɴ�С��˳���� ��
��3��B��CԪ�ص�ijЩ�⻯��ķ����о�����18�����ӣ���B�������⻯��Ļ�ѧʽ����B��C����Щ�⻯��ķе����ϴ����Ҫԭ���� ��
��4��A��B��D���γɷ���ʽΪA2BD��ij�������û����������Bԭ�ӵĹ���ӻ���������1mol�÷����к��Цм�����Ŀ�� ��
��5��C��F��Ԫ���γɵ�ij������ľ����ṹ��ͼ��ʾ����û�����Ļ�ѧʽ�� �� Cԭ�ӵ���λ���� �� 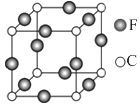
���𰸡�
��1��1s22s22p63s23p63d10{��[Ar]3d10}
��2��N��O��C
��3��C2H6�������⻯�N2H4�����Ӽ�������
��4��sp2��1mol
��5��Cu3N��6
���������⣺A��B��C��D��E��F����Ԫ�ؾ�λ�����ڱ���ǰ�����ڣ���ԭ��������������Ԫ��A��ԭ�Ӱ뾶��С��Ԫ�أ���A��HԪ�أ�BԪ�ػ�̬ԭ�ӵĺ�����ӷ�ռ�ĸ�ԭ�ӹ�����ܼ�������BΪCԪ�أ�DԪ��ԭ�ӵ��ѳɶԵ���������δ�ɶԵ���������3������D��OԪ�أ�CԪ��ԭ����������B��С��D����C��NԪ�أ�E��D����ͬһ���壬��E��SԪ�أ�Fλ��ds������ԭ�ӵ������ֻ��1�����ӣ���FΪCuԪ�أ���1��Cu+��Cuԭ��ʧȥ�������ӵõ������ӣ������Ӻ�����28�����ӣ����ݹ���ԭ����д��ͭ���Ӻ�������Ų�ʽΪ1s22s22p63s23p63d10{��[Ar]3d10}���ʴ�Ϊ��1s22s22p63s23p63d10{��[Ar]3d10}����2��B��C��D�ֱ���C��N��OԪ�أ���λ��ͬһ���ڣ�ͬһ����Ԫ�ص�һ����������ԭ��������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ�����������Ԫ�ص�һ�����ܴ�С˳����N��O��C���ʴ�Ϊ��N��O��C����3��C��NԪ�ص�ijЩ�⻯��ķ����о�����18�����ӣ���B�������⻯��ΪC2H6��
����������⻯���۷е�ϸߣ������⻯���к��������̼���⻯���в�����������Ե����⻯���۷е�ϸߣ�
�ʴ�Ϊ��C2H6�������⻯�N2H4�����Ӽ�����������4��H��C��O���γɷ���ʽΪH2CO��ij�����ΪHCHO���÷�����Cԭ�Ӽ۲���ӶԸ�����3�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Cԭ���ӻ���ʽΪsp2��һ����ȩ�����к���1���м�����1mol��ȩ�к���1mol�м���
�ʴ�Ϊ��sp2��1mol����5��N��Cu��Ԫ���γɵ�ij������ľ����ṹ��ͼ��ʾ���þ�����Cuԭ�Ӹ���=12�� ![]() =3��Nԭ�Ӹ���=8��
=3��Nԭ�Ӹ���=8�� ![]() =1�������仯ѧʽΪCu3N���þ�����Nԭ����λ��Ϊ6��
=1�������仯ѧʽΪCu3N���þ�����Nԭ����λ��Ϊ6��
�ʴ�Ϊ��Cu3N��6��
A��B��C��D��E��F����Ԫ�ؾ�λ�����ڱ���ǰ�����ڣ���ԭ��������������Ԫ��A��ԭ�Ӱ뾶��С��Ԫ�أ���A��HԪ�أ�BԪ�ػ�̬ԭ�ӵĺ�����ӷ�ռ�ĸ�ԭ�ӹ�����ܼ�������BΪCԪ�أ�DԪ��ԭ�ӵ��ѳɶԵ���������δ�ɶԵ���������3������D��OԪ�أ�CԪ��ԭ����������B��С��D����C��NԪ�أ�E��D����ͬһ���壬��E��SԪ�أ�Fλ��ds������ԭ�ӵ������ֻ��1�����ӣ���FΪCuԪ�أ���1��Cu+��Cuԭ��ʧȥ�������ӵõ������ӣ������Ӻ�����28�����ӣ����ݹ���ԭ����д��ͭ���Ӻ�������Ų�ʽ����2��B��C��D�ֱ���C��N��OԪ�أ���λ��ͬһ���ڣ�ͬһ����Ԫ�ص�һ����������ԭ��������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ���3��C��NԪ�ص�ijЩ�⻯��ķ����о�����18�����ӣ���B�������⻯��Ϊ���飻
����������⻯���۷е�ϸߣ���4��H��C��O���γɷ���ʽΪH2CO��ij�����ΪHCHO���÷�����Cԭ�Ӽ۲���ӶԸ�����3�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Cԭ���ӻ���ʽ��һ����ȩ�����к���1���м�����5��N��Cu��Ԫ���γɵ�ij������ľ����ṹ��ͼ��ʾ�����þ�̯�ּ���þ�����N��Cuԭ�Ӹ������Ӷ�ȷ���仯ѧʽ���þ�����Nԭ����λ��Ϊ6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֲ�ͬ�ѻ���ʽ�Ľ�������ľ�����ͼ��ʾ���й�˵������ȷ���� ( )

A����Ϊ�������ѻ�����Ϊ�������ܶѻ�����Ϊ���������ѻ�����Ϊ�����������ܶѻ�
B��ÿ���������е�ԭ�����ֱ�Ϊ����1������2������2������4��
C��������ԭ�ӵ���λ���ֱ�Ϊ����6����8����12����12
D���ռ������ʵĴ�С��ϵΪ����<��<�ۣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ������С��36��X��Y��Z��W��R����Ԫ�أ�ԭ������������������Ԫ���У���RΪ����Ԫ�أ���ԭ������Ϊ27��X�۵����Ų�ʽΪnsnnpn �� Ԫ��Z��̬ԭ��s����������p����������ȣ�W����������Ԫ���ܲ�����ͬ����δ�ɶԵ�����ĿΪ1���� �����жϳ���Ԫ�ػش��������⣺
��1����̬Rԭ�Ӻ�������Ų�ʽΪ �� X��Y��Z����ԭ�ӵ�һ�������ɴ�С��˳��Ϊ���þ���Ԫ�ط��ű�ʾ����
��2��1mol�����[R��XY��6]4���к��ЦҼ�����ĿΪ ��
��3��XZW2��һ�ָ߶������ʣ��ṹ���ȩ���ƣ�Xԭ���ӻ���ʽΪ �� ��е���ڼ�ȩ����Ҫԭ���� ��
��4��YW3Ϊ��ɫ����״�����д̼�����ζ��Һ�壬�÷��ӵ����幹��Ϊ����������������
��5��ij����ľ����ṹ��ͼ��ʾ����û�����Ļ�ѧʽΪ��R��Z�þ���Ԫ�ط��ű�ʾ���� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£�����ѡ������ʾ�����ʼ�ת������ͨ��һ����Ӧʵ�ֵ��ǣ� ��
A.0.1 mol?L��1 HC1 ![]() ?C12
?C12 ![]() ?Ca��ClO��2��aq��
?Ca��ClO��2��aq��
B.Al3+ ![]() ?A1O2��
?A1O2�� ![]() ?Al��OH��3
?Al��OH��3
C.A1 ![]() ?NaA1O2��aq��
?NaA1O2��aq�� ![]() ?NaAlO2��s��
?NaAlO2��s��
D.MgO��s�� ![]() ?Mg��NO3��2��aq��
?Mg��NO3��2��aq�� ![]() ?Mg��s��
?Mg��s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵͼ�У�A��һ�����Σ�B����̬�⻯�C�ǵ��ʣ�F��ǿ�ᡣ��X������ǿ�ỹ��ǿ��ʱ��������ת����ϵ(�������P��Ӧ��������������ȥ)����X��ǿ��ʱ��������B��Cl2��Ӧ������C�⣬��һ�����������Ρ�
![]()
����˵��������ȷ����( )
A����X��ǿ��ʱ��A��B��C��D��E��F�о���ͬһ��Ԫ�أ�F������H2SO4
B����X��ǿ��ʱ��A��B��C��D��E��F�о���ͬһ��Ԫ�أ�F��HNO3
C����X��ǿ��ʱ��C�ڳ���������̬����
D��B��Cl2�ķ�Ӧ��������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������
��1�������£�0.1mol/LHCl��Һ��pH=��0.005mol/LBa��OH��2��Һ��pH=��
��2�������£�pH=13��Ba��OH��2��ҺaL��pH=3��H2SO4��ҺbL��ϣ���Ϻ���Һ����仯���Բ��ƣ�
�������û����Һ�����ԣ���a��b=��
�������û����ҺpH=12����a��b= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�HNO3���������ԣ��������Ե���
A. C��HNO3 B. FeO��HNO3 C. Fe2O3��HNO3 D. CuO��HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�е�Ԫ�ؼ��仯�����ת����ϵ���ж�����˵������ȷ���ǣ� �� 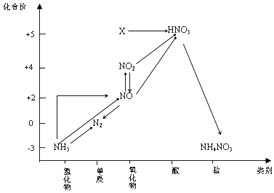
A.X��N2O5
B.�����ſ������ռ�NO����
C.��ҵ����NH3��������ˮΪԭ����������
D.��NH3��N2 �� ��ԭ���Ͽ���NH3����NO2��Ӧʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���þ۹��ֵ�Ͳ�������з�ɢϵ�����ܹ۲쵽�����ЧӦ���ǣ� ��
A.Fe(OH)3����
B.��������Һ
C.KOH��Һ
D.������Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com