
【题目】下列有关化合物的说法正确的是( )
A.干冰的主要成分是H2O
B.SO2可大量用于漂白食品
C.吸入CO可导致人体中毒
D.小苏打的主要成份是Na2CO3
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡. I.已知H2A在水中存在以下平衡:H2AH++HA﹣ , HA﹣H++A2﹣ .
(1)NaHA溶液(选填“显酸性”、“显碱性”、“显中性”或“无法确定”).
(2)某温度下,0.1mol/L的NaHA溶液,下列关系中,一定正确的是 .
A.c(H+)c(OH﹣)=1×10﹣14
B.c(Na+)+c(H+)=c(HA﹣)+2c(A2﹣)
C.c(Na+)>c(HA﹣)>c(A2﹣)>c(H2A)
D.c(Na+)=c(HA﹣)+c(A2﹣)+c(H2A)
(3)已知常温下,H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2﹣(aq)△H>0. ①降低温度时,Ksp(填“增大”、“减小”或“不变”,下同).
②滴加少量浓盐酸,c(Ca2+) .
③测得25℃时,CaA的Ksp为2.0×10﹣11 , 常温下将10g CaA固体投入100mL CaCl2溶液中,充分搅拌后仍有固体剩余,测得溶液中c(Ca2+)=0.1mol/L,则溶液中c(A2﹣)=mol/L
(4)II.工业废水中常含有一定量的Cr2O72﹣和CrO42﹣ , 它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有还原沉淀法,该法的工艺流程为: CrO42﹣ ![]() Cr2O72﹣
Cr2O72﹣ ![]() Cr3+
Cr3+ ![]() Cr(OH)3
Cr(OH)3
其中第①步存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O
若平衡体系的pH=2,则溶液显色.
第②步中,还原1mol Cr2O72﹣离子,需要mol的FeSO47H2O.
第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)Cr3+(aq)+3OH﹣(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)c3(OH﹣)=10﹣32 , 要使c(Cr3+)降至10﹣5mol/L,溶液的pH应调至 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在第3周期中,置换酸中氢的能力最强的元素的元素符号为______,化学性质最稳定的元素符号是________,最高价氧化物的水化物的酸性最强的化合物的化学式是_______,碱性最强的化合物的化学式是___________,显两性的氢氧化物的化学式是____________,该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为_______________________________、_________________________________,原子半径最大的金属元素的名称是____________________,离子半径最小的离子结构示意图是 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 25℃时,pH均为1的盐酸和醋酸加水稀释1000倍,所得溶液的pH:醋酸>盐酸
B. 等体积、等物质的量浓度的NH4HSO4和KOH溶液混合:c(K+)=c(SO42-)>c(NH4+)>c(OH-)>c(H+)
C. 25℃时,pH=12的氨水和pH=2的盐酸等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. 浓度均为0.1 molL-1的HClO溶液和NaClO溶液等体积混合,溶液中有下列关系:c(HC1O)+2c(H+)=c(C1O-)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2molH2完全燃烧生成水蒸气放出热量484kJ,且1molH—H键断裂时吸收热量为436kJ, 水蒸气中1molH—O键形成时放出热量463kJ,则O2中1molO=O键完全断裂时吸收热量( )
A.496 kJB.188 kJC.557 kJD.920kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将amolN2与bmH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值__________。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数为25%。计算平衡时NH3的物质的量为_________________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同),n(始):n(平)=______。
(4)原混合气体中,a:b=______________。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某溶液中加入BaCl2溶液,再加入稀盐酸至溶液呈中性,有白色沉淀产生.该溶液一定含有( )
A.CO32﹣
B.OH﹣
C.SO42﹣
D.HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率可用于衡量电解质溶液导电能力的大小,且电导率越大溶液的导电能力越强。室温下 ,用0.l00 mol·L-1的NH3· H2O 滴定10 .00mL 浓度均为0 . 100 mol·L-1HCl和CH3COOH的混合液,电导率曲线如图所示。下列说法正确的是
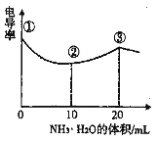
A.① 溶液中c(H +)为0 . 200 mol·L-1
B.溶液温度高低为① >③ >②
C.③ 点后因离子数目减少使电导率略降低
D.③ 点时溶液中有c ( C1一)>(CH3 COO一)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种气态烃组成的混合物,体积为10ml与过量的氧气混合再充分燃烧,将生成物通过浓H2SO4气体体积减少15ml,再通过碱石灰气体体积又减少20ml [气体体积均为同温(120℃)同压(101kPa)]。混合烃的组成可能为( )
A. C2H6和C2H4 B. C2H4和C2H2 C. CH4和C3H4 D. C4H10和C2H4[来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com