
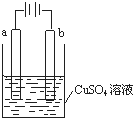
| A. | 若a和b为石墨,通电后a电极上发生的反应为Cu2++2e-═Cu | |
| B. | 若a和b为铜,通电后a电极有气体产生 | |
| C. | 若a为铜,b为铁,通电后Cu2+向a电极移动 | |
| D. | 若a为粗铜,b为纯铜,通电后b电极质量增加 |
分析 A.电解池中如果石墨作电极,则阳极上阴离子放电;
B.电解池中如果铜作电极,则阳极上铜本身失电子;
C.电解池中阳离子向阴极移动;
D.粗铜的精炼中,粗铜作阳极,纯铜作阴极,阴极上铜离子放电.
解答 解:A.电解池中如果石墨作电极,则a极上的电极反应式为4OH--4e-=O2↑+2H2O,故A错误;
B.电解池中如果铜作电极,则阳极上铜本身失电子,所通电后a电极没有气体产生,故B错误;
C.该电解池中,铜离子向阴极即b极附近移动,故C错误;
D.若a为粗铜,b为纯铜,该装置是铜的精炼,通电后b电极上铜离子放电生成铜单质,所以质量增加,故D正确;
故选D.
点评 本题考查电解池原理,注意电解池中,活泼金属和惰性电极作阳极时的区别,为易错点.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | |
| B. | 饱和FeCl3溶液在20℃时呈现棕黄色,100℃呈现红褐色,不能用平衡移动原理来解释 | |
| C. | 在$\frac{{c({H^+})}}{{c(O{H^-})}}$=10-12.溶液中Na+、I-、NO3-、SO42-能大量共存 | |
| D. | 在原电池装置中,电子从负极流出,沿导线流入正极,经溶液或盐桥回到负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是能起银镜反应的物质一定是醛 | |
| B. | 乙烯和甲苯都能使酸性高锰酸钾溶液褪色 | |
| C. | 苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸 | |
| D. | 在酯化反应中,羧酸脱去羧基中的氢原子,醇脱去羟基生成水和酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
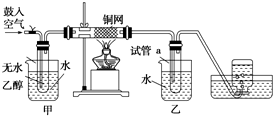 某实验如图.
某实验如图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com