
【题目】某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
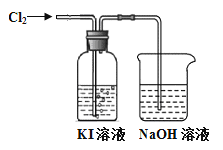
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)已知I2+I-![]() I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
操作 | 实验现象 | |
a | 取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色, 水层显浅黄色。 |
b | 取2~3 mL饱和碘水,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色,水层几近无色。 |
① 实验b的目的是 。
② 根据实验a中,水层中含有的粒子有 。
③ 实验a中水溶液颜色变浅的原因是 。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为 。
(2)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化。已知1 mol Cl2可氧化0.2 mol I2,该反应的化学方程式是 。
(3) 根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为 。
【答案】(1)① 对比实验,证明实验a中水层显浅黄色是因为存在I2+I-![]() I3-平衡,不是单一的I2浓度降低所导致的。(2分)
I3-平衡,不是单一的I2浓度降低所导致的。(2分)
② I2、I-、I3-、Cl-、K+(可不写H2O、H+、OH-)(2分)
③ 由于萃取使水溶液中I2浓度降低,同时I2+I-![]() I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
④ 取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(2分)
【或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。】
(2)I2+5Cl2+6H2O ![]() 10H Cl +2 H IO3(2分)
10H Cl +2 H IO3(2分)
(3)溶液先变蓝后褪色(1分)
【解析】
试题分析:(1)① 实验b的目的是对比实验,证明实验a中水层显浅黄色是因为存在I2+I-![]() I3-平衡,不是单一的I2浓度降低所导致的。
I3-平衡,不是单一的I2浓度降低所导致的。
② 根据实验a中,取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。因为KI+Cl2![]() 2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I-
2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I-![]() I3-,对可逆反应I2、I-、I3-均存在;
I3-,对可逆反应I2、I-、I3-均存在;
③ 实验a中水溶液颜色变浅的原因是由于萃取使水溶液中I2浓度降低,同时I2+I-![]() I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充检验I-或I2的实验,所以答案是取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。)
(2)已知1 mol Cl2可氧化.2 mol I2,知Cl2和I2的系数比是5:1,根据氧化还原反应特点,化合价升降总数相等,判断出I2变为+5价,配平得I2+5Cl2+6H2O ![]() 10HCl +2H IO3;
10HCl +2H IO3;
(3)向淀粉-KI溶液中持续通入氯气,可能观察到的现象为溶液先变蓝,I2+5Cl2+6H2O ![]() 10HCl +2HIO3所以后褪色;
10HCl +2HIO3所以后褪色;


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. ![]() C和
C和![]() C是碳元素的2种核素,它们互为同位素
C是碳元素的2种核素,它们互为同位素
B. 化学研究者开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与C60互称同素异形体
C. 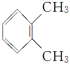 与
与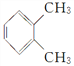 互为同分异构体
互为同分异构体
D. 硝基苯可看成是由![]() 和—NO2两种基团组成
和—NO2两种基团组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均三甲苯(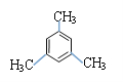 )是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,主要用于制备合成树脂、抗氧化剂等。
)是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,主要用于制备合成树脂、抗氧化剂等。
(1)均三甲苯属于苯的同系物,选用一种试剂区别苯和均三甲苯两种液体,这种试剂是_____________________。
(2)均三甲苯分子中的一个氢原子被氯原子取代所得产物有__________种。
(3)三聚氰胺( )也是一种重要的化工原料,其结构可看作均三甲苯分子中的部分碳原子被N原子置换所得。三聚氰胺的分子式_____________,其核磁共振氢谱有________个峰,含氮的质量分数为_____________。
)也是一种重要的化工原料,其结构可看作均三甲苯分子中的部分碳原子被N原子置换所得。三聚氰胺的分子式_____________,其核磁共振氢谱有________个峰,含氮的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl![]() 2ClO2↑+Cl2↑+2NaCl+2H2O
2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4![]() 2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2↑+O2↑+Na2SO4+2H2O
(1)方法一的离子方程式:__;
(2)方法二中被氧化的物质是______,若反应中有0.1 mol电子转移,则产生的ClO2气体在标准状况下的体积为______L;
在下面的化学方程式上用单线桥法标出电子转移的方向和数目:________________
2NaClO3+H2O2+H2SO4![]() 2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2↑+O2↑+Na2SO4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
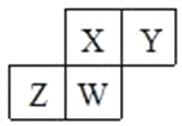
A. 原子半径:Z>W>X>Y
B. 元素X、Z的最高化合价分别与其主族序数相等
C. 最高价氧化物对应水化物的酸性:Y>X>W
D. 最简单气态氢化物的热稳定性:Y>X>W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碘水倒入汽油中,下列现象描述正确的是( )
A. 汽油在上层,水在下层,汽油无色
B. 汽油在下层,水在上层,汽油紫色
C. 汽油在上层,水在下层,水无色
D. 水在上层,汽油在下层,汽油紫色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com