
【题目】(1)除去Na2CO3粉末中混入的NaHCO3杂质用__方法,化学方程式为__。
(2)除去氧化铜粉末中混入的氧化铝粉末通常用__试剂,离子方程式为__。
【答案】加热 2NaHCO3![]() Na2CO3+ CO2↑+H2O NaOH溶液 Al2O3+2OH-=2AlO2-+H2O
Na2CO3+ CO2↑+H2O NaOH溶液 Al2O3+2OH-=2AlO2-+H2O
【解析】
根据碳酸氢钠的不稳定性和氧化铝的两性分析解答。
(1)碳酸氢钠不稳定,加热分解,可通过加热的方法除去Na2CO3粉末中混入的NaHCO3杂质,反应的化学方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:加热;2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:加热;2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)氧化铝具有两性,与强碱反应,可用氢氧化钠溶液除去氧化铜粉末中的氧化铝,离子方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:NaOH溶液;Al2O3+2OH-=2AlO2-+H2O。


科目:高中化学 来源: 题型:
【题目】室温下,0.1 mol/L 的某二元酸 H2A 溶液中,可能存在的所有含 A 粒子的物质的量分数随 pH 变化的关系如图所示。下列说法不正确的是

A.H2A 的电离方程式:H2A=H+ + HA-
B.NaHA 溶液显酸性
C.等物质的量浓度的 NaHA 和Na2A 溶液等体积混合,离子浓度大小关系为:c(Na+)>c(A2-)>c(HA-)
D.pH = 5 时,在NaHA 和 Na2A 的混合溶液中: c(HA-) : c(A2-)= 100:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】痛灭定钠是一种吡咯乙酸类的非甾体抗炎药,其合成路线如图:
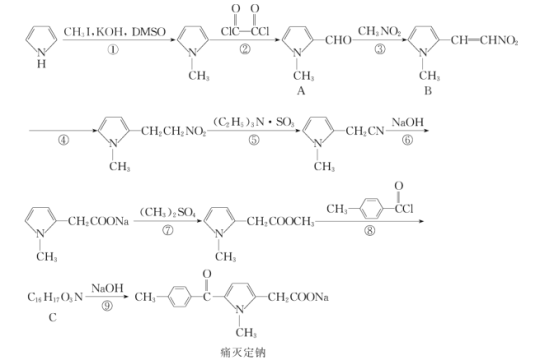
回答下列问题:
(1)化合物B中含有官能团的名称是__。
(2)化学反应①和④的反应类型分别为__和__。
(3)化合物C的结构简式为__。
(4)下列关于痛灭定钠的说法错误的是__。
a.与溴充分加成后官能团种类数不变
b.能够发生水解反应
c.核磁共振氢谱分析能够显示6个峰
d.可使溴的四氯化碳溶液褪色
e.1mol痛灭定钠与氢气加成最多消耗3molH2
(5)反应⑦的化学方程式为__。
(6)芳香族化合物X的相对分子质量比A大14,写出遇FeCl3溶液显紫色且取代基仅位于苯环对位上化合物X的结构简式:__(不考虑立体异构)。
(7)根据该试题提供的相关信息,写出由化合物![]() 及必要的试剂制备有机化合物
及必要的试剂制备有机化合物![]() 的合成路线图。__。
的合成路线图。__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A.含有4molHCl的浓盐酸与足量MnO2反应,生成1molCl2
B.常温常压下,16gO2所含的电子数为8NA
C.标准状况下,22.4LSO3中所含的SO3分子数为NA
D.78gNa2O2与足量水充分反应时电子转移数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列四个反应:①2Na+2H2O=2NaOH +H2↑;②2Na2O2+2H2O=4NaOH+O2↑;③2F2+2H2O=4HF+O2;④2H2O![]() 2H2↑ +O2↑
2H2↑ +O2↑
(1)水只做氧化剂的是__;
(2)水只做还原剂的是__;
(3)水既做氧化剂又做还原剂的是__;
(4)水既不做氧化剂又不做还原剂的是__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当实验出现某种现象时,即可判定该步实验操作已完成。下列实验中出现结束该步操作的现象正确的是
A.“镀锌铁皮锌镀层厚度的测定”:铁皮在稀硫酸溶液中不再产生气泡
B.“食醋总酸含量的测定”:滴入NaOH标准溶液,锥形瓶内溶液恰好呈浅红色
C.“乙酸乙酯碱性条件下水解”:NaOH溶液上层的油层消失
D.“硫酸亚铁铵的制备”:蒸发![]() 和
和![]() 混合溶液,出现大量晶体
混合溶液,出现大量晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。

请回答下列问题
(1)写出下列物质的化学式A___,E___。
(2)F在空气中转化为G的化学方程式:__。
(3)A和B反应的化学方程式:___。
(4)H和I生成J的离子方程式:___。
(5)如何检验E中大量存在的阳离子?__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法正确的是( )
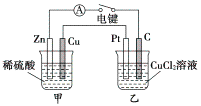
A. 甲装置是电解池,乙装置是原电池
B. 当甲中产生0.1 mol气体时,乙中析出固体的质量为6.4 g
C. 实验一段时间后,甲烧杯中溶液的质量减小
D. 将乙中的C电极换成铜电极,则乙装置可变成电镀装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意计算填空。
(1)在标准状况下,8.5g某气体占有的体积为5.6L,则该气体的摩尔质量是__。
(2)在标准状况下,0.01mol某气体的质量为0.28g,则该气体的相对分子质量为__,该气体的密度为__g·L1。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合物中CO和CO2物质的量之比是__,C和O原子个数比是__,CO的质量分数是__。
(4)现有mg某气体,它由双原子分子构成,它的相对分子质量为M。若阿伏伽德罗常数用NA表示,则:该气体的物质的量为__mol;该气体所含原子总数为__个;该气体在标准状况下的体积为__L;该气体溶于水后形成1L溶液(该气体不与水反应),其物质的量浓度为__mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com