
Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是
A.Na2FeO4处理水时,既能杀菌,又能在处理水时产生胶体净水
B.Na2FeO4既是氧化产物又是还原产物
C.Na2O2在上述反应中只作氧化剂
D.2 mol FeSO4发生反应时,共有10 mol电子发生转移
C
【解析】
试题分析:根据题给反应判断,反应中FeSO4中铁元素的化合价由+2价升高到+3价,Na2O2中氧元素的化合价既升高又降低。A、Na2FeO4处理水时,Na2FeO4具有强氧化性能杀菌,其还原产物氢氧化铁又能在处理水时产生胶体净水,正确;B、反应中FeSO4→Na2FeO4,铁元素的化合价升高,Na2FeO4是氧化产物,Na2O2→Na2FeO4,氧元素化合价降低,Na2FeO4是还原产物,正确; C、Na2O2中氧元素的化合价既升高又降低,既作氧化剂又作还原剂,错误;D、反应中化合价升高的元素有Fe,由+2价→+6价,氧元素,由-1价→0价,2molFeSO4发生反应时,共有2mol×4+1mol×2=10mol电子转移,正确。
考点:考查氧化还原反应基本概念。


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内物质),能使溶液恢复到原来的成分和浓度的是
A.AgNO3[AgNO3] B.NaOH[NaOH]
C.KCl[KCl] D.CuSO4[CuO]
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列有关说法错误的是
A.医药中常用酒精消毒,是因为酒精能使细菌蛋白质变性
B.聚酯纤维、光导纤维都属于有机高分子材料
C.对废旧电池回收处理是为了防止重金属污染水源和土壤
D.绿色化学的核心是从源头上减少和消除化工生产对环境的污染
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:填空题
(12分)A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:
元素 | A | B | C | D | E |
性质 或结 构信 息 | 室温下单质呈气态,原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,乙具有弱酸性 | 单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体 | E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分 |
试回答以下问题
(1)B在周期表中的位置是 ,B的氢化物与E的氢化物比较,沸点较高的是 (填化学式)。
(2)D3B可与水反应生成2种碱性物质,请写出这一化学方程式 。
(3)写出丙的电子式为 。并说明丙在空气中漂白的原理(用化学方程式表示) 。(请参考下表数据)
酸 | 电离常数 |
HClO | Ka=3.0×10-8 |
H2CO3 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
(4)由A、B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成深绿色溶液,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程中,下列说法中不正确的是
A.上述过程中,最终被还原的是NO3—
B.从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4
C.假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1∶1
D.上述过程中,会产生一种无色无味的难溶于水的气体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是
A.p (Ne) < p (H2) < p (O2) B.p (H2) < p (O2) < p (Ne)
C.p (O2) < p (Ne) < p (H2) D.p (H2) < p (Ne) < p (O2)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:填空题
(10分)甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,A和B都极易溶于水,用玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟。各物质之间存在如下图所示的转化关系:

请回答下列问题:
(1)丙与A反应生成乙和C的化学反应方程式为——————
(2)向0.1 mol/L的C溶液中通入A至显中性,溶液中各离子浓度由大到小的顺序为:__________.
(3)常温下取M的饱和溶液与AgI的饱和溶液等体积混合,再加入足量的AgNO3浓溶液发生反应,则生成沉淀的物质的量较多的是________。(填化学式)
(4)电解尿素[CO(NH2)2]的碱性溶液制取甲的装置示意图如右图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。

电解时,b极的电极反应是_______。若在a极产生112mL气体(标准状况),则消耗尿素的质量为______g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:实验题
(14分)某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
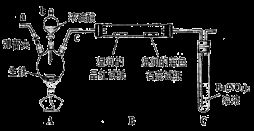
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为_____________:实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为_______________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是________________________________。

(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是_____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:选择题
如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是
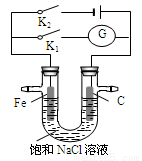
A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com