
| A. | 碘单质的升华 | B. | NaCl溶于水 | ||
| C. | 将金属Mg加热变为气态 | D. | NH4Cl受热分解 |
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:解答题
 .
. 名称是2,4二甲基-4-乙基庚烷.
名称是2,4二甲基-4-乙基庚烷. )的官能团的名称为碳碳双键、羟基.
)的官能团的名称为碳碳双键、羟基. .
. 形成六元环酯的反应
形成六元环酯的反应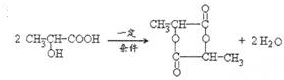 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠投入硫酸铜溶液中:2Na+Cu2+═2Na++Cu | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ | |
| D. | 碳酸氢钠溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①:除去Cl2中含有的少量HCl | |
| B. | 装置②:构成锌-铜原电池 | |
| C. | 装置③:可用于比较碳酸与苯酚的酸性强弱 | |
| D. | 装置④:验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li在氧气中燃烧能生成Li2O2 | |
| B. | 将SO2通入过量FeCl3和BaCl2的混合溶液中可生成BaSO4沉淀 | |
| C. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后最终溶液呈红色 | |
| D. | 将稀硫酸滴加到Fe(NO3)2溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质Cl2、Br2、I2的氧化性强弱 | |
| B. | 气态氢化物NH3、H2O、HF的稳定性 | |
| C. | 碱金属单质Li、Na、K与水反应的剧烈程度 | |
| D. | 1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量就是物质的质量 | |
| B. | 摩尔是国际单位制七个基本单位之一 | |
| C. | 摩尔是粒子的数量单位 | |
| D. | 阿伏伽德罗常数约为6.02×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com