
| ① |
| 2 |
| ② |
| 2 |
| -196.6 |
| 2 |
| -113 |
| 2 |


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
| A、氧气的摩尔质量是32g |
| B、1mol二氧化碳的质量为44g?mol-1 |
| C、O2的摩尔质量(单位是g?mol-1)在数值上等于其相对分子质量 |
| D、不同物质的摩尔质量一定不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B、不慎将硫酸沾在皮肤上,立刻用干布擦净,然后用氢氧化钠溶液冲洗 |
| C、实验室配制一定物质的量浓度的溶液,定容时仰视刻度线,所配制溶液浓度偏大 |
| D、某溶液中加入BaC12溶液,产生了不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(I-)/mol?L-1 | c(Fe3+)/mol?L-1 | v/mol?L-1?s-1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2>I2>S |
| B、H2S>NaI>H2O |
| C、S>I2>O2 |
| D、H2O>NaI>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称量25.20gNaCl |
| B、用10mL的量筒量取6.25mL的Na2CO3溶液 |
| C、用25mL滴定管量取14.80mL溶液 |
| D、用广泛pH试纸测得溶液的pH为12.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
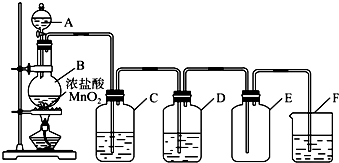
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L HCl和0.1 mol/L H2SO4与2 mol/L NaOH溶液反应,其反应速率相同 |
| B、大理石块与大理石粉分别同0.1 mol/L盐酸反应,其反应速率相同 |
| C、Mg、Al在相同条件下分别与0.1 mol/L盐酸反应,其反应速率相同 |
| D、0.1 mol/L HCl和0.1 mol/L HNO3与相同形状和大小的大理石反应,其反应速率相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com