
| A. | 0.3mol O2和 0.3mol H2O | |
| B. | 0.1mol H2SO4和3.6g H2O | |
| C. | 0.1mol MgSO4•7H2O和0.1mol C12H22O11(蔗糖) | |
| D. | 6.02×1023个CO2与0.1mol KMnO4 |
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的分子构成计算.
解答 解:A.0.3 mol O2含有0.6molO,0.3 mol H2O含有0.3molO,二者不同,故A错误;
B.0.1 mol H2SO4含有0.4molO,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,含有0.2molO,二者不同,故B错误;
C.0.1 mol MgSO4•7H2O含有1.1molO,0.1 mol C12H22O11(蔗糖)含有1.1molO,氧原子的物质的量相同,故C正确;
D.6.02×1023个CO2为1mol,含有2molO,0.1 mol KMnO4含有0.4molO,二者不同,故D错误.
故选C.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的计算能力的考查,本题注意把握物质的构成特点,为本题考查的侧重点,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | A1(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
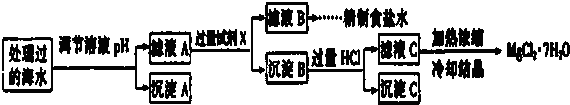
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加催化剂,使N2和H2在一定条件下转化为NH3 | |
| B. | 增大压强,有利于SO2和O2反应生成SO3 | |
| C. | 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| D. | 黄绿色的氯水光照后颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .塑料制品是人类日常生活中使用量最大的合成高分子材料.大量塑料制品的生产和使用,给人们的生活带来了极大的方便,同时也造成了严重的环境问题--白色污染.当今白色污染问题已得到了人们应有的重视,一些科学家也成功地寻找到了治理白色污染的有效途径.结合学过的知识,回答下列问题:
.塑料制品是人类日常生活中使用量最大的合成高分子材料.大量塑料制品的生产和使用,给人们的生活带来了极大的方便,同时也造成了严重的环境问题--白色污染.当今白色污染问题已得到了人们应有的重视,一些科学家也成功地寻找到了治理白色污染的有效途径.结合学过的知识,回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃不能发生加成反应,烯烃不能发生取代反应 | |
| B. | 符合通式CnH2n+2的一定是烷烃,符合通式CnH2n的一定是烯烃 | |
| C. | 能发生加成反应的一定是烯烃 | |
| D. | 烷烃中含饱和键、烯烃、炔烃中含不饱和键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com