
| A、滴加少量NaOH溶液,促进CH3COOH的电离,溶液的pH降低 |
| B、当V=20mL,溶液中存在:c(Na+)-c(CH2COO)+c(CH3COOH) |
| C、当V=20mL,NaOH与CH3COOH恰好反应时,所得溶液pH=7 |
| D、当0<V<20mL时,溶液中一定存在:c(Na+)>c(CH2COO)>c(OH)>c(H+) |


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
 太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.
太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容器内压强不随时间变化 |
| B、容器内各物质的浓度不随时间变化 |
| C、容器内X、Y、Z的浓度之比为1:2:3 |
| D、单位时间消耗0.1 mol X同时生成0.3 mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③ | C、③④ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:

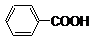

查看答案和解析>>
科目:高中化学 来源: 题型:
 元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.
元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.| 80℃通电 |
| Ⅰ |
| 室温,KCl |
| Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH2═CH2+H2O
| |||
B、CH4H10
| |||
C、CH3CH3+Br2
| |||
D、2C2H2+5O2
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com