
| A. | 原子序数:b>a>c>d | B. | 原子半径:A>B>C>D | ||
| C. | 金属性:B>A,非金属性:D>C | D. | 离子半径:D>C>B>A |
分析 aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),原子序数:b>a>c>d,A、B同周期,C、D同周期,且A、B在周期表中C、D的下一周期,由形成的离子可知,A、B为金属,C、D为非金属性,结合元素周期律递变规律解答该题.
解答 解:aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),原子序数:b>a>c>d,A、B同周期,C、D同周期,且A、B在周期表中C、D的下一周期,由形成的离子可知,A、B为金属,C、D为非金属性,
A.aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),则有原子序数:b>a>c>d,故A正确;
B.A、B在周期表中C、D的下一周期,并且原子序数:b>a>c>d,原子核外电子层数越多,原子半径越大,同周期元素原子序数越大,原子半径越小,则有原子半径:A>B>D>C,故B错误;
C.A、B为金属,原子序数:b>a,金属性:A>B,而C、D为非金属,原子序数c>d,非金属性C>D,故C错误;
D.aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,核电荷数越大离子半径越小,核电荷数b>a>c>d,故离子半径dD(n+1)->cCn->aAn+>bB(n+1),故D错误,
故选A.
点评 本题考查位置结构性质关系及应用,关键是根据核外电子排布确定元素所在周期表中的位置,在根据元素周期律的递变规律是解答,难度不大.


科目:高中化学 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | Zn+Fe2+=Zn2++Fe | ||
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe3+具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、NO2、N2、粉尘 | B. | CO2、Cl2、N2、雾 | C. | SO2、NO2、CO、烟尘 | D. | CO2、NO、NH3、H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A2B3 | B. | BA2 | C. | AB4 | D. | B3A2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
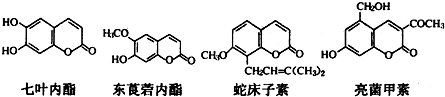
| A. | 七叶内酯与东茛菪内酯互为同系物 | |
| B. | 四种化合物含有的官能团种类完全相同 | |
| C. | l mol上述四种物质与足量氢氧化钠溶液反应,消耗氢氧化钠最多的是亮菌甲素 | |
| D. | 它们都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7:2 | B. | 2:7 | C. | 1:2 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲、乙中铝都有剩余 | |
| B. | 铝片的质量是5.4 g | |
| C. | 盐酸或氢氧化钠的物质的量浓度为0.1 mol/L | |
| D. | 盐酸或氢氧化钠的物质的量浓度为0.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com