
分析 (1)C与水反应生成CO和氢气;
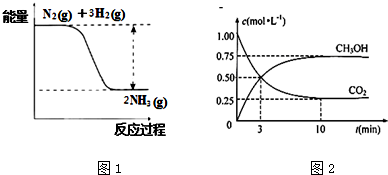
(2)①由图可知,反应物的总能量大于生成物的总能量;断裂化学键吸收能量,生成化学键释放能量;
②结合平衡时正逆反应速率相等、各组分的浓度不变等及其衍生的一些物理量分析;
(3)由图2可知,甲醇的浓度变化量为0.75mol/L,根据v=$\frac{△c}{△t}$计算v(CH3OH),再利用速率之比等于化学计量数之比计算v(H2),相同条件下气体压强之比等于气体物质的量之比.
解答 解:(1)C与水反应生成CO和氢气,反应为C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO (g)+H2(g),
故答案为:C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO (g)+H2(g);
(2)①由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应,断裂化学键吸收能量,生成化学键释放能量,△H=断裂化学键吸收能量-生成化学键释放能量<0,可知断裂化学键吸收能量小于生成化学键释放能量,
故答案为:放热;小于;
②A.由于气体的质量以及容器的体积不变,则容器中混合气体的密度不随时间变化,不能用于判断是否达到平衡,故A错误;
B.单位时间内断裂3mol H-H键的同时断裂6mol N-H键,说明正逆反应速率相等,达到平衡状态,故B正确;
C. 因不能确定起始配比数、转化率以及平衡常数,则N2、H2、NH3的物质的量之比为1:3:2不能说明达到平衡状态,故C错误;
D.容器中混合气体的平均相对分子质量不随时间变化,说明气体的物质的量不变,达到平衡状态,故D正确.
故答案为:AC;
(3)①由图2可知,10min达平衡时甲醇的浓度变化量为0.75mol/L,所以v(CH3OH)=$\frac{0.75mol/L}{10min}$=0.075mol/(L•min),速率之比等于化学计量数之比,所以v(H2)=3v(CH3OH)=3×0.075mol/(L•min)=0.225mol/(L•min),
故答案为:0.225mol/(L.min);
②反应前后气体压强之比等于其物质的量之比,反应前气体物质的量=4mol,甲醇生成0.75mol,最后达到平衡状态二氧化碳物质的量0.25mol,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),
起始量(mol) 1 3 0 0
变化量(mol) 0.75 2.25 0.75 0.75
平衡量(mol) 0.25 0.75 0.75 0.75
达平衡时容器内平衡时与起始时的压强之比=(0.25+0.75+0.75+0.75):(1+3)=5:8=0.625,
故答案为:5:8 (或0.625).
点评 本题考查较为综合,为高考常见题型,侧重于学生的分析、计算能力,化学图象分析、化学平衡状态的判断、化学平衡状态的判定等,注重高频考点的考查,有利于基础知识和基本能力的培养,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/s c/(mol•L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol•L-1) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/(mol•L-1) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室中酒精灯着火,立即用水扑灭 | |
| B. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| C. | 皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗 | |
| D. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①中溶液变黄,③中溶液橙色加深 | |
| B. | ②中Cr2O72-被C2H5OH氧化 | |
| C. | 对比②和④可知K2Cr2O7酸性溶液氧化性强 | |
| D. | 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100℃时,某溶液pH=6,则该溶液一定显酸性 | |
| B. | 25℃时,0.1mol/L的NaHSO3溶液pH=4,溶液中c(SO32-)<c(H2SO3) | |
| C. | 25℃时,pH=3的硫酸溶液与pH=11的氨水等体积混合,所得溶液呈酸性 | |
| D. | 室温下,10mL0.1mol/L CH3COOH溶液与5mLO.lmol/LNaOH溶液混合,所得溶液中有:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com