
| ||
| ||
| 11.2L |
| 22.4L/mol |
| 16g |
| 100g |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,Na2CO3生成的CO2多 |
| B、两者的水溶液都是呈现碱性,可以使无色的酚酞变红色 |
| C、加热时,Na2CO3难分解,但NaHCO3容易分解 |
| D、同温度下,Na2CO3在水中的溶解度比NaHCO3大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、④⑤⑥ |
| C、①③④ | D、②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
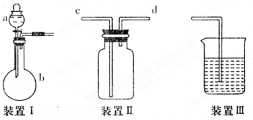 某实验小组利用如图所示装置完成有关实验.
某实验小组利用如图所示装置完成有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
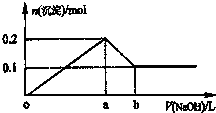 在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是( )
在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是( )| A、混合溶液中Al3+的物质的量为0.1mol |
| B、NaOH的浓度为0.5 mol/L |
| C、在b点处溶液中的溶质只有NaAlO2 |
| D、图中线段oa:ab=4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、48 | B、55 | C、95 | D、198 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com