
【题目】已知化合物A与B、丙与丁的元素组成相同,且四种物质中都含有同一种元素。A与B在常温下均呈液态。D为应用最广泛的金属,且D与甲的浓溶液在常温作用无明显现象,加热时有大量气体产生。(相关转化部分反应条件和生成物未标出)。
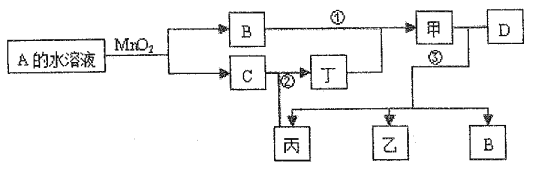
注:转化关系中,②表示C与丙反应生成丁。
(I)反应中MnO2的作用为_____,有1molA完全反应生成B、C转移____mol电子;
(II)若反应①除生成甲外,还生成丙,回答(1)、(2)小题:
(1)反应②的化学方程式:_______________。
(2)写出过量D与甲的稀溶液反应的离子方程式:____________。
(III)若丙为无色有刺激性气味的气体,可以使品红溶液褪色,回答(3)、(4)小题:
(3)写出下列化学方程式②:__________________;③(甲足量):_________________。
(4)检验乙溶液中离子的实验方法为______________。
【答案】 催化剂 1 2NO+O2==2NO2 3Fe+8H++2NO3-==3Fe2++2NO↑+4H2O 2SO2+O2![]() 2SO3 2Fe+6H2SO4(浓)
2SO3 2Fe+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2↑+3H2O Fe3+:取样于一干净试管中,加入少量KSCN溶液,溶液变红;SO42-:取样,先加入稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀
Fe2(SO4)3+3SO2↑+3H2O Fe3+:取样于一干净试管中,加入少量KSCN溶液,溶液变红;SO42-:取样,先加入稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀
【解析】化合物A与B在常温下均呈液态,由图中转化关系可知,A为H2O2、B为H2O、C为O2,D为应用最广泛的金属,D为Fe,Fe与甲的浓溶液在常温下无明显现象,加热时有大量气体产生,甲可能为硫酸或硝酸。
(I). H2O2在MnO2催化作用下分解生成水和O2,MnO2的作用为催化剂,反应的化学方程式为2H2O2![]() 2H2O+O2↑,在该反应中,氧元素的化合价部分从-1价升高到0价,部分从-1价降低到-2价,1molH2O2完全反应时转移电子1mol,故答案为:催化剂;1;
2H2O+O2↑,在该反应中,氧元素的化合价部分从-1价升高到0价,部分从-1价降低到-2价,1molH2O2完全反应时转移电子1mol,故答案为:催化剂;1;
(II). (1). 若反应①除生成甲外,还生成丙,则甲为硝酸、丙为NO、丁为NO2、乙为Fe(NO3)2或Fe(NO3)3,反应②为NO和O2反应生成NO2,化学方程式为2NO+O2=2NO2,故答案为:2NO+O2=2NO2;
(2). 过量的Fe与稀硝酸反应生成Fe(NO3)2、NO和H2O,离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
(III). (3). 若丙为无色有刺激性气味的气体,可以使品红溶液褪色,则甲为硫酸、丙为SO2、丁为SO3、乙为Fe2(SO4)3,反应②为SO2和O2在催化剂作用下加热反应生成SO3,化学方程式为2SO2+O2![]() 2SO3,反应③为足量的浓硫酸与Fe反应生成硫酸铁、二氧化硫和水,化学方程式为2Fe+6H2SO4(浓)
2SO3,反应③为足量的浓硫酸与Fe反应生成硫酸铁、二氧化硫和水,化学方程式为2Fe+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2↑+3H2O,故答案为:2SO2+O2
Fe2(SO4)3+3SO2↑+3H2O,故答案为:2SO2+O2![]() 2SO3;2Fe+6H2SO4(浓)
2SO3;2Fe+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2↑+3H2O;
Fe2(SO4)3+3SO2↑+3H2O;
(4). 乙为Fe2(SO4)3溶液,Fe3+的检验方法为:取少量乙溶液置于一干净试管中,加入少量KSCN溶液,溶液变红,说明含有Fe3+;SO42-的检验方法为:取少量乙溶液置于一干净试管中,先加入稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀生成,说明含有SO42-,故答案为:Fe3+ :取样于一干净试管中,加入少量KSCN溶液,溶液变红;SO42-:取样,先加入稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】在溶液中可进行反应A+B![]() C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是
C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是

A. 该反应是吸热反应
B. 反应速率最大的时间段是在t1~t2
C. 四个时间段内生成C的量最多的是t1~t2
D. 反应速率后来减慢主要是受反应物浓度变化的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干燥的氨气在高温下能被氧化铜氧化,生成两种单质和一种化合物。完成上述反应可选用下列装置进行。
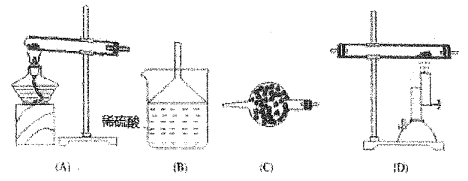
(1)当气体流向从左到石时,仪器连接的顺序是___________。
(2)装置B中试剂的作用是_________,装置C的作用是______。
(3)装置D 中反应的化学方程式是__________。
(4)装置A 中反应的化学方程式是_________ 。
(5)若实验室要收集氨气,选择E装置时,棉花的作用为_________,选择F 装置时,氨气应从______口进。
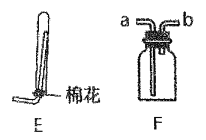
(6)工业制备氨气的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:2CH3COOK+2H2O ![]() CH3CH3↑+2CO2↑+H2↑+2KOH现有下列衍变关系(A、B、C、D、E、F、G均为有机物): 回答下列问题:
CH3CH3↑+2CO2↑+H2↑+2KOH现有下列衍变关系(A、B、C、D、E、F、G均为有机物): 回答下列问题: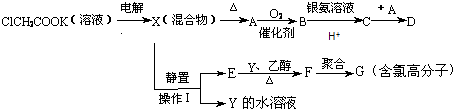
(1)电解ClCH2COOK溶液时阳极的电极反应式是(填选项).
A.2ClCH2COO﹣﹣2e﹣=ClCH2CH2Cl+2CO2↑
B.2H++2e﹣=H2↑
C.2H2O+2e﹣=2OH﹣+H2↑
D.4OH﹣﹣4e﹣=2H2O+O2↑
(2)操作Ⅰ的名称是 , G的结构简式是 .
(3)写出B与银氨溶液按物质的量1:4反应的化学方程式: .
(4)写出下列化学方程式并指出其反应类型:A→B方程式: .
E→F方程式: .
指出反应类型:A→B , E→F .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置制取NH3,并用AlCl3溶液吸收多余NH3制Al(OH)3,最后回收NH4Cl,能达到实验目的的是

A. 用装置甲制取NH3
B. 用装置乙吸收NH3制取Al(OH)3
C. 用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌
D. 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
A. NH3、NO2、N2 B. NH3、NO、CO2
C. NH3、NO2、CO2 D. NO、CO2、N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com