
【题目】某有机物的结构如图所示,下列关于该有机物的描述不正确的是
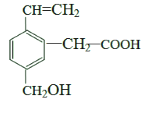
①所有碳原子可能共面;
②能使酸性KMnO4溶液和溴水褪色,且原理相同;
③1mol该有机物分别与足量Na或NaHCO3反应,产生气体在相同条件下体积不相等;
④能发生酯化反应;
⑤能发生加聚反应;
⑥1mol该有机物完全燃烧生成CO2和H2O消耗O2的体积为280 L(标准状况)
A. ①②B. ②⑥C. ③⑥D. ②③
【答案】D
【解析】
①有机物结构中苯环、双键为平面结构,与苯环、双键直接相连的原子一定共面,则分子中所在的碳原子可能共面,故不选①;
②该有机物含有碳碳双键,发生氧化反应使酸性KMnO4溶液褪色,使溴水褪色是发生加成反应,原理不同,故选②;
③-COOH、-OH均可与Na反应生成氢气,则1mol该有机物与足量Na反应生成1mol氢气;与NaHCO3反应的只有-COOH,1mol该有机物与足量-COOH反应生成1mol二氧化碳,在相同条件下,气体体积相同,故选③;
④该有机物含有羧基,羟基,可以发生酯化反应,故不选④;
⑤该有机物含有碳碳双键,可以发生加聚反应,故不选⑤;
⑥该有机物分子式为C11H12O3,1mol该有机物完全燃烧生成CO2和H2O消耗O2的体积为(11+3-1.5)mol×22.4L/mol=280 L,故不选⑥;
综上所述,应选②③,故本题正确答案为D。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
【题目】把0.4molX气体和0.6molY气体混合于2L密闭容器中,使它们发生如下反应:4X(g)+5Y(g) ![]() nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为_______________。
(2)2min末时Y的浓度为_____________________________。
(3)化学反应方程式中n=_____________________________。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的__________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应伴随能量变化,其中能量的主要形式是热能。
I:如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,往试管中放入几小块镁片,再用滴管滴入5mL盐酸于试管中,试回答下列问题:
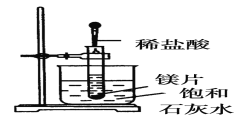
(1)实验中观察到的现象是________________________。
(2)产生上述现象的原因是________________________。
(3)写出有关反应的离子方程式__________________________。
(4)由实验推知,MgCl2和H2的总能量________(填“大于”“小于”或“等于”)镁片和HCl的总能量。
II:从能量变化的角度研究反应:2H2+O2=2H2O。
(1)如图能正确表示该反应中能量变化的是_________。
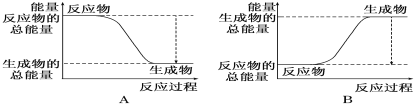
(2)已知断开或形成1 mol化学键吸收或放出的能量,叫做该化学键的键能,单位为kJ·mol-1。一些键能数据如下表:
化学键 | H—H | O=O | H—O |
键能(kJ·mol-1) | 436 | 496 | 463 |
请回答:
断裂反应物2 mol H2和1 mol O2的化学键,需要_______的总能量为______kJ;形成生成物2 mol H2 O的化学键,需要______的总能量为______kJ。所以该反应能量变化值的大小 ____________ kJ(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在如图所示转化关系(部分生成物和反应条件略去);已知A 由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:
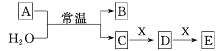
(1)若A为单质,且C为一元强酸。
①化合物B 的结构式为_______。
②写出一种工业制备单质A的离子方程式:________。
③X可能为______(填字母代号)。
a.NaOH b.AlCl3 c.Na2CO3 d.Na[Al(OH)4]
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A的电子式为______。
②A与H2O反应的化学方程式为_____。
③室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸是咖啡的热水提取液成分之一,结构简式如下图,关于绿原酸判断正确的是( )

A.1 mol绿原酸与足量NaHCO3溶液反应,生成3 mol CO2气体
B.1 mol绿原酸与足量溴水反应,最多消耗2.5 mol Br2
C.1 mol绿原酸与足量NaOH溶液反应,最多消耗4 mol NaOH
D.绿原酸水解产物均可以与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法,正确的是
A.用图1装置制取干燥纯净的NH3 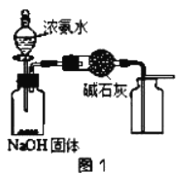
B.用图2装置实验室制备Fe(OH)2 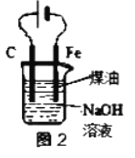
C.用图3装置可以完成“喷泉”实验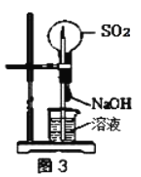
D.用图4装置测量Cu与浓硝酸反应产生气体的体积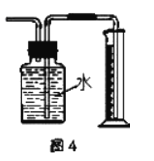
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A分子由C、H、O三种元素组成,其相对分子质量为120,0.1molA在足量的氧气中充分燃烧后生成0.8mol CO2 和7.2g H2O;A可以发生银镜反应,其苯环上的一卤代物有三种。
(1)A的分子式是_________,A中含氧官能团的名称是________________,A的结构简式是_______________。
已知:I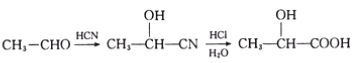
II.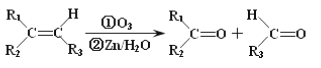
现有如下转化关系:
![]()
其中D能使溴的四氯化碳溶液褪色,F继续被氧化生成G,G的相对分子质量为90。
(2)C可能具有的化学性质是____________。(请填字母)
① 能与H2发生加成反应;② 能在碱性溶液中发生水解反应;③ 能与甲酸发生酯化反应;④ 能与Ag(NH3) 2OH溶液发生银镜反应;⑤能与氢氧化钠溶液反应
A.①②③ B.①③⑤ C.①②③⑤ D.②③④⑤
(3)① 写出C→D的化学反应方程式是________________________________________;反应类型是____________。
②在催化剂条件下,C生成高聚物的化学方程式是_________________________________。
(4)请写出化合物C可能的同分异构体结构简式是___________________________。须同时符合下列条件:
①属于酯类化合物;
②遇三氯化铁溶液显紫色;
③与新制氢氧化铜悬浊液共热可生成红色沉淀;
④苯环上的一卤代物只有一种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,由于石油价格的不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成线路。

请回答下列问题:
(1)写出反应类型:反应①______________,反应②__________________。
(2)写出结构简式:PVC________________,C______________________。
(3)写出A![]() D的化学方程式_______________________________。
D的化学方程式_______________________________。
(4)与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合物),写出其中一种的结构简式_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,参照元素在表中的位置,回答下列问题:
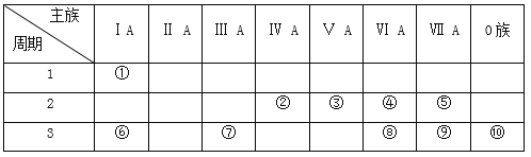
(1)上述元素最高价氧化物对应水化物中,酸性最强的是__________(填化学式),碱性最强的是__________(填化学式),显两性的是__________(填名称)。
(2)气态氢化物中,最稳定的是__________(填化学式),④⑧形成的氢化物中沸点最高的是__________(填化学式),原因是__________________。
(3)④分别和①、⑥两种元素的原子按1:1组成的常见化合物的电子式分别为__________和_______。用电子式表示②和④的三原子分子的形成过程____________。
(4)④⑥⑦⑨的简单离子半径由大到小的顺序为__________(用离子符号和“>”表示)。
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式___________。
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是______。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com