
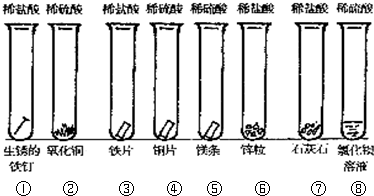


科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 |
| B.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性 |
| C.浓硫酸和浓硝酸都具有强氧化性 |
| D.硫酸和硝酸都是重要的化工原料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液质量都增大 |
| B.溶液质量都减小 |
| C.溶液中溶质的质量分数都增大 |
| D.溶液中溶质的质量分数都减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下铝或铁质的容器可贮运浓硝酸和浓硫酸,是因为常温下铝或铁与浓硝酸和浓硫酸不反应 |
| B.铵态氮肥不能与碱性肥料混合使用,是因为它们能相互反应,使有效氮损失 |
| C.浓硝酸需要用棕色瓶保存,是因为它见光易分解 |
| D.工业浓硝酸通常呈黄色,是由于硝酸溶液中溶解了硝酸分解所产生的二氧化氮 |
查看答案和解析>>
科目:高中化学 来源:期中题 题型:实验题
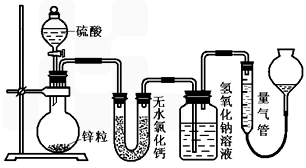
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向鸡蛋清溶液中,加入(NH4)2SO4溶液 | 有白色沉淀产生 | 蛋白质发生了变性 |
| B | 向某溶液中加入BaCl2溶液 | 有白色沉淀产生 | 生成难溶于水的BaSO4,该溶液中一定含有硫酸根离子 |
| C | 向苯中滴入少量浓溴水震荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性味的气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硝酸保存在无色玻璃试剂瓶中 |
| B.氢氧化钠溶液保存在有橡皮塞的玻璃试剂瓶中 |
| C.在蔗糖中滴加浓硫酸,蔗糖变黑是因为浓硫酸具有脱水性 |
| D.常温下浓硫酸可以用铝罐储存,是因为铝能在冷的浓硫酸中钝化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com