
【题目】卤素单质从F2到I2在常温常压下的聚集状态由气态、液态到固态的原因是( )
A.原子间的化学键键能逐渐减小
B.范德华力逐渐增大
C.原子半径逐渐增大
D.氧化性逐渐减弱
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】30.工业上通过电解饱和的食盐水来制取氯气。现取500ml含NaCl为11.7g的饱和食盐水进行电解,
(1)在标准状况下制得Cl2多少升?
(2)所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:SO2(g)+ ![]() O2(g)SO3(g)△H=﹣98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
O2(g)SO3(g)△H=﹣98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
A.98.32kJ
B.196.64kJ/mol
C.<196.64kJ
D.>196.64kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,化学实验是化学学习的重要内容。
(1)以下是实验室常用的部分仪器。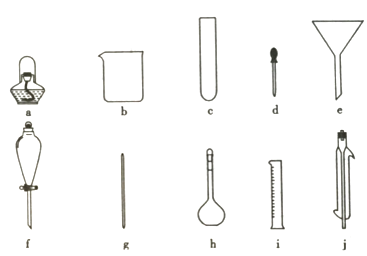
①仪器f和j的名称分别为、。
②在分液操作中,必须用到的仪器是(填字母,下同)。
③能作反应容器且可直接加热的仪器是。
④过滤时,需要用到的玻璃仪器是
(2)下列实验操作的叙述中,正确的是______(填字母)。
A.将用水润湿的pH试纸浸入稀盐酸中,测定溶液的pH
B.用稀盐酸洗涤盛放过石灰水的试剂瓶
C.稀释浓硫酸时,可先在烧杯中加入一定体积的浓硫酸,再在搅拌下慢慢加入水
D.各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知含氧酸可用通式XOm(OH)n表示,如X是S,m=2,n=2,则这个式子表示为H2SO4 . 一般而言,该式子中m大的是强酸,m小的是弱酸.下列各含氧酸中酸性最强的是( )
A.HClO3
B.H2SeO3
C.H3PO4
D.HMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:SO32﹣>I﹣ . 向含有amolKI和amolK2SO3的混合液中通入bmolCl2充分反应(不考虑Cl2与I2之间的反应).下列说法不正确的是( )
A.当a≥b时,发生的离子反应为SO32﹣+Cl2+H2O=SO42﹣+2H++2Cl﹣
B.当5a=4b时,发生的离子反应为SO32﹣+2I﹣+5Cl2+4H2O=4SO42﹣+I2+8H++10Cl﹣
C.当a≤b≤ ![]() a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D.当a<b< ![]() a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于四种基本反应类型,但属于氧化还原反应的是
A. Fe+CuSO4=FeSO4+Cu B. 2KMnO4===K2MnO4+MnO2+O2↑
C. CO+CuO===Cu+CO2 D. MnO2+4HCl(浓)===MnCl2+Cl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活.
已知:
①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l);△H=﹣2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H= .
(2)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2﹣ . 在电池内部O2﹣移动方向和在电池负极反应的物质分别是
A.正极;O2
B.负极;C3H8
C.正极;C3H8
D.负极;O2
(3)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO (g)+H2O(g)CO2(g)+H2 (g)
①下列事实能说明该反应达到平衡的是 .
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
②T℃时,在1L的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如表:
时间/min | c(CO) | c(H2O)(g) | c(CO2) | c(H2) |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | 0.100 | 0.200 | 0.100 | 0.100 |
4 | 0.100 | 0.200 | 0.100 | 0.100 |
计算2min内用CO表示的该反应速率v=;4min时保持其它条件不变,向上述平衡体系中加入0.1molCO、0.1molCO2、0.1molH2 , 此时反应将向向进行(填“正”或“逆”).
③已知420℃时,该化学反应的平衡常数为9.如果反应开始时CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 . 又知397℃时该反应的平衡常数为12,请判断该反应的△H0 (填“>”、“=”、“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)在一密闭容器中有如下反应:mA(g)+nB(g)pC(g)△H.某化学兴趣小组根据此反应在不同条件下的实验数据,作出了如图曲线图: 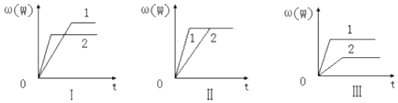
其中,ω表示C在反应混合物中的质量分数,t表示反应时间.其它条件不变时,下列分析正确的是( )
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1 , m+n<p
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2 , m+n=p
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2 , △H<0
D.若m+n<p,△H>0,则该反应在低温下容易自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com