
向2 L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15 s阶段n(B)未画出]。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同。已知t3~t4阶段为使用催化剂。观察下图,回答以下问题:

(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为________。
(2)图乙中t2时引起平衡移动的条件是________,t5时引起平衡移动的条件是________。
(3)图乙中表示平衡混合物中,在这四个阶段中C的含量最高的一段时间是________。
(4)该反应的化学方程式可以表示为:
________________________________________________________________________,
正反应为________(填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为________。
答案 (1)0.004 mol·L-1·s-1
(2)增加A的浓度 升高温度
(3)t5~t6
(4)3A(g)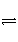
 B(g)+2C(g) 吸热
B(g)+2C(g) 吸热
(5)0.04 mol
解析 (1)根据图甲v(C)= =0.004 mol·L-1·s-1。
=0.004 mol·L-1·s-1。
(2)分析图乙,t2时刻,v(正)突然增加,v(逆)逐渐增加,所以t2时刻增加了A的量;t3~t4阶段使用了催化剂;由于四个阶段所改变的外界条件均不同,t4时刻改变的条件可能为压强或温度,改变温度时平衡一定会发生移动,而t4时刻平衡未发生移动,只是速率减小,所以t4时刻改变的条件是压强,且为降压;t5时刻正逆反应速率突然升高,改变条件为升温。
(3)图乙中t2~t3,t5~t6,v(正)>v(逆),其余时间段v(正)=v(逆),所以C的含量最高的一段时间为t5~t6段。
(4)降压由于平衡不移动,所以此反应前后气体分子数不变。由图甲可求出v(A)=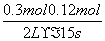 =0.006 mol·L-1·s-1,即
=0.006 mol·L-1·s-1,即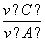 =
= ,所以此反应的化学方程式为3A(g)
,所以此反应的化学方程式为3A(g)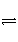
 B(g)+2C(g);升高温度时,v(正)>v(逆),平衡正向移动,所以正反应为吸热反应。
B(g)+2C(g);升高温度时,v(正)>v(逆),平衡正向移动,所以正反应为吸热反应。
(5)由于化学方程式可知,15 s时,B的物质的量增加了0.06 mol,所以开始时加入的B的物质的量为0.1 mol-0.06 mol=0.04 mol。


科目:高中化学 来源: 题型:
向过氧化氢溶液中逐渐滴入FeCl2溶液,可能观察到的现象有( )
 A.有白色沉淀生成,溶液颜色由浅绿色变棕色
A.有白色沉淀生成,溶液颜色由浅绿色变棕色
B.有红褐色沉淀生成,上层溶液呈棕黄色
C.有无色无味的气体产生,该气体能使带火星的木条复燃
D.能看到溶液颜色加深,既无沉淀产生,也无气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
现有室温下的四种溶液,其pH如下表所示,下列有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
A.③④中分别加入适量醋酸钠晶体,两溶液pH均增大
B.②③两溶液等体积混合,所得溶液中:c(H+)>c(OH-)
C.分别加水稀释10倍,溶液的pH:①>②>④>③
D.V1L④和V2L①溶液混合后,若pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.非自发反应在任何条件下都不能实现
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.凡是放热反应都是自发的,吸热反应都是非自发的
D.熵增加且放热的反应一定是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列有关图象,说法正确的是( )

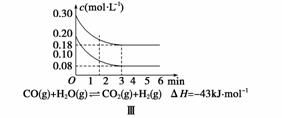
A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
B.由图Ⅱ知,反应在t6时刻,NH3体积分数最大
C.由图Ⅱ知,t3时采取增大反应体系压强的措施
D.图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
①结构相似的有机物是同系物 ②分子组成相差一个或几个CH2原子团的有机物是同系物 ③若烃中碳、氢元素的质量分数相同,它们必定是同系物
A.①②③ B.只有②③
C.只有③ D.只有①③
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下1.68 L某可燃气体在足量氧气中完全燃烧,将产物通入足量澄清石灰水,得到白色沉淀质量15.0 g,若用足量碱石灰吸收燃烧产物,质量增加9.3 g,则该可燃气体为( )
A.C2H4 B.C3H6
C.C2H2 D.C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化工生产原理错误的是
( )。
A.可以用电解熔融的氯化钠的方法来制取金属钠
B.可以用钠加入氯化镁饱和溶液中制取镁
C.用电冶铝时,原料是氯化铝
D.高炉炼铁需要高温,但其中所发生的反应不一定都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处,请用相应的化学用语回答下列问题:
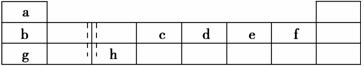
(1)写出仅由e形成的两种带有相同电荷数的阴离子的符号________、
________。
(2)d元素名称为____,其双原子分子的电子式为________。

Ⅰ Ⅱ
(3)左图Ⅰ是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表
Ar,则其中柱形“8”代表的是(填化学式)____晶体,1 mol该晶体中含有
____mol化学键。
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(左图Ⅱ)中序列“5”的氢化物
的名称是____,空间构型为________;序列“2”的氢化物的结构式是________,
属于____(填“极性”或“非极性”)分子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com