
【题目】A、B都是短周期元素,原子最外层电子排布式分别为![]() 。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。
。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。
(1)比较电离能:
①![]() _____
_____ ![]() (填“>”或“<”,下同)
(填“>”或“<”,下同)
②![]() _____
_____ ![]() 。
。
(2)通常A元素的化合价是 _____________ ,对A元素呈现这种价态进行解释:
①用原子结构的观点进行解释:_____________ 。
②用电离能的观点进行解释:______________ 。
(3)写出D跟水反应的离子方程式: _________ 。
【答案】< < +1 钠原子失去一个电子后核外电子排布式为ls22s22p6,原子轨道处于全充满状态,该+1价阳离子体系能M低,极难再失去电子 Na原子的第一电离能相对较小,第二电离能比第一电离能大很多,通常Na原子只能失去一个电子 ![]()
【解析】
A、B都是短周期元素,原子最外层电子排布式分别为(n+1)sx、nsx+1npx+3,故x+1=2,解得x=1,故A的外层电子排布式分别为(n+1)s1,处于第ⅠA族,B外层电子排布式分别为ns2np4,处于第ⅥA族,A与B可形成化合物D,D溶于水时有气体逸出,该气体能使带火星的木条复燃,该气体为O2,故化合物D为Na2O2,A为Na,B为O,结合物质性质与元素周期律解答。
(1)同周期自左而右,第一电离能呈增大的趋势,同主族自上而下第一电离能减小。O失去一个电子比Na困难得多,故电离能I1(Na)<I1(O);He是稀有气体元素,原子核外最外层达到了稳定结构,很难失去电子,故I1(O)<I1(He);
(2)Na元素的化合价是+1,
①钠原子失去一个电子后形成电子排布为1s22s22p6,原子轨道全充满的+1价阳离子,该离子结构体系能量低,极难再失去电子,故通常化合价为+1;
②Na原子的第一电离能相对较小,第二电离能比第一电离能大很多倍,通常Na原子只能失去一个电子,化合价为+1价;
③过氧化钠跟水反应生成氢氧化钠与氧气,反应离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】PET(![]() ,M链节= 192 g·mol1)可用来生产合成纤维或塑料。测某PET样品的端基中羧基的物质的量,计算其平均聚合度:以酚酞作指示剂,用c mol·L1 NaOH醇溶液滴定m g PET端基中的羧基至终点(现象与水溶液相同),消耗NaOH醇溶液v mL。下列说法不正确的是
,M链节= 192 g·mol1)可用来生产合成纤维或塑料。测某PET样品的端基中羧基的物质的量,计算其平均聚合度:以酚酞作指示剂,用c mol·L1 NaOH醇溶液滴定m g PET端基中的羧基至终点(现象与水溶液相同),消耗NaOH醇溶液v mL。下列说法不正确的是
A.PET塑料是一种可降解高分子材料
B.滴定终点时,溶液变为浅红色
C.合成PET的一种单体是乙醇的同系物
D.PET的平均聚合度![]() (忽略端基的摩尔质量)
(忽略端基的摩尔质量)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1 mol·L-1 KOH 溶液滴定 10 mL 0.1 mol·L-1 HA(Ka =1.0×10-5)溶液的滴定曲线如图所示。下列说法正确的是( )
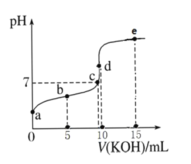
A.a 点溶液的 pH 约为 5
B.水的电离程度:c 点>d 点
C.b 点溶液中粒子浓度大小: c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
D.e 点溶液中:c(K+)=2c(A-)+2c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从_______ (填“接头流向水表”或“水表流向接头”)。

(2)某二次电池放电的电池反应为2Fe+O2+2H2O = 2Fe(OH)2。反应结束时,电极a的质量__________(填“减小”“不变”或“增加”),该电池的正极反应式为____________。

(3)有如图装置:

①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为_______________;Q点时,a电极收集到的气体体积为________________。

②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入5 mol CO和4 mol NO,发生反应: 2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH1=-746.5 kJ/mol,图1为平衡时NO的体积分数与温度、压强的关系。同时为探究催化剂对CO、NO转化率的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。下列说法中正确的是
N2(g)+2CO2(g) ΔH1=-746.5 kJ/mol,图1为平衡时NO的体积分数与温度、压强的关系。同时为探究催化剂对CO、NO转化率的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。下列说法中正确的是
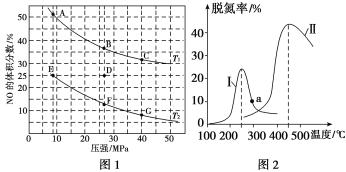
A.温度:T1<T2
B.若在D点对反应容器降温的同时缩小体积使体系压强增大,重新达到的平衡状态可能是图中G点
C.E点时NO的平衡转化率为50%
D.a点是对应温度下的平衡脱氮率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的操作、现象和结论都正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向浓度均为0.10molL-1的KCl和KI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
B | 向Na2SO3溶液中先加入Ba(NO3)2溶液,然后再加入稀盐酸 | 生成白色沉淀,加入稀 盐酸,沉淀不溶解 |
|
C | 向盛有NH4Al(SO4)2溶液的试管中,滴加少量NaOH溶液 | 产生使湿润的红色石蕊试纸变蓝的气体 | NH4++OH- = NH3↑+H2O |
D | 测定等物质的量浓度的Na2CO3和NaClO的pH值 | Na2CO3>NaClO | 酸性:H2CO3<HClO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的K2S、KOH混合溶液中滴加稀盐酸至过量。其中主要含硫各物种(H2S、HS、S2)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出)。下列说法不正确的是
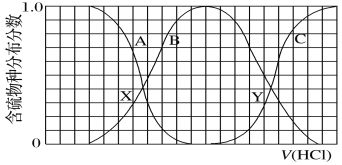
A.A曲线表示S2-随盐酸加入量增加时的分布分数改变情况
B.X、Y为曲线两交叉点。若已知Y点处的pH,则可计算Ka1(H2S)
C.X、Y点对应溶液中水的电离程度大小关系为:X<Y
D.Y点对应溶液中c(K+)与含硫各微粒浓度的大小关系为:c(K+)=3[c(H2S)+c(HS)+c(S2)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有关文献的理解错误的是
A. 《汉书》中“高奴县有洧水可燃”,《梦溪笔谈》对“洧水”的使用有“试扫其烟为墨,黑光如漆,松墨不及也”的描述,其中的烟指炭黑
B. 《物理小识》记载“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不茂”,青矾厂气是CO和CO2
C. 《本草纲目》描述“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”其中的碱是K2CO3
D. 《天工开物》记裁制造青瓦“(窑)泥周寒其孔,浇水转釉”,红瓦转化为青瓦的原因是Fe2O3转化为其他铁的氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为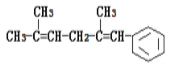 ,判断下列说法中不正确的是( )
,判断下列说法中不正确的是( )
A.它可以使酸性KMnO4溶液褪色
B.它可发生取代反应、加成反应、加聚反应、氧化反应
C.1mol该有机物燃烧消耗氧气为18.5mol
D.它与氢气发生加成反应,最多可以消耗4mol氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com