
【题目】下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
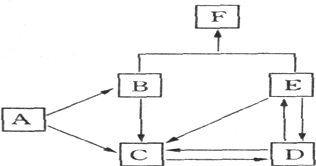
据此,请回答下列问题:
(1)写出以下物质的化学式:A________,D______,F__________。
(2)写出下列变化的化学方程式:
B→C______________________________________________
E→C______________________________________________
【答案】N2 NO2 NH4NO3 4NH3+5O2 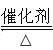 4NO+6H2O 3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
4NO+6H2O 3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
【解析】
由题意中各物质均含有相同的元素,而F可用作氮肥,可知各物质均含有N元素,A是单质,则A为N2,D在常温下呈气态,C、D、E之间可以相互转化,且A能转化为B和C,而B与E可以得到氮肥F,可推知B为NH3,C为NO,D为NO2,E为HNO3,F是NH4NO3。
(1)由上述分析可知,A为N2,D为NO2,F是NH4NO3,故答案为:N2;NO2;NH4NO3;
(2)B→C的反应为在催化剂作用下,氨气与氧气共热反应生成一氧化氮和水,反应的化学方程式为4NH3+5O2  4NO +6H2O;E→C的反应为铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O。
4NO +6H2O;E→C的反应为铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O。


科目:高中化学 来源: 题型:
【题目】将2×10- 5mol/LKCl 与2×10- 5mol/LAgNO3溶液等体积混合,下列说法正确的是 (已知AgCl 的Ksp=1.8×10-10 )
A.有AgCl沉淀析出B.无AgCl沉淀析出
C.无法确定有无AgCl沉淀析出D.有沉淀但不是AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学习小组的同学设计用分子筛催化CH4还原NO2并检验还原产物。回答下列问题:
(1)甲组同学设计用如图所示装置分别制备CH4和NO2。
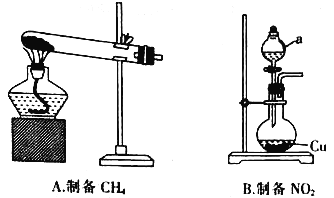
①在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3的化学方程式为___________。
②仪器a的名称为__________,仪器a中的药品是__________(填名称)。__________(填“能”或“不能”)用铁代替圆底烧瓶中的铜。
(2)乙组同学利用甲组制得的干燥气体并利用下列装置用CH4还原NO2
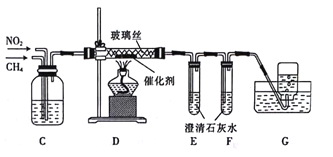
①C装置的作用是______________(列举2点)。
②D装置反应管中盛放玻璃丝的目的是___________;CH4与NO2生成N2和CO2的化学方程式为_____________。
③E装置中澄清石灰水未变浑浊,F装置中澄清石灰水变浑浊,其原因可能是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
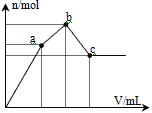
A. a点对应的沉淀只有BaSO4
B. b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-==Al(OH)3↓+2BaSO4↓
C. c点溶液呈碱性
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)分析该反应并回答下列问题:
①该反应的平衡常数表达式为K=____________。
②下列选项能判断该反应达到平衡状态的依据有__________(填序号)。
A.2v(正)(H2)= v(逆)(CO)
B.一定条件下,单位时间内消耗2molH2的同时生成 1mol CH3OH
C.恒温、恒容时,容器内的压强不再变化
D.恒温、恒容时,容器内混合气体的密度不再变化
E.混合气体的平均相对分子质量不随时间而变化
(2))下图是该反应在不同温度下CO转化率随时间的变化曲线:

①该反应的△H________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1 ________ K2(填“>”、“<”或“=”)。
(3)某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为________________。
(4)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式________________________。
(5)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为__________(填 化学式,下同),c 口通入的物质为__________。 ②该电池正极的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断A(g)+B(g) ![]() C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
A. 压强不随时间改变
B. 气体的密度不随时间改变
C. c(A)不随时间改变
D. 单位时间里生成C和D的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈现周期性变化的根本原因是
A. 原子半径呈周期性变化
B. 元素化合价呈周期性变化
C. 电子层数逐渐增加
D. 元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=___________________。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率______(填“增大”“减小”或“不变”),原因是_____________________________________________________________。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各4/3mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验操作及现象能得出相应结论的是
操作 | 现象 | 结论 | |
A. | 将蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液一定为浓盐酸 |
B. | 向 CH3COONa 溶液中滴入酚酞试液,加热 | 加热后红色加深 | CH3COONa 水解是吸热反应 |
C. | 向某溶液中加入盐酸,将产生 的气体通入澄清石灰水 | 澄清石灰水变浑浊 | 该溶液中一定有 CO32— |
D. | 向 NaCl 溶液中滴加过量 AgNO3 溶液,再滴加 KI 溶液 | 先出现白色沉淀, 后出现黄色沉淀 | Ksp(AgI) < Ksp(AgCl) |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com