

分析 (1)根据碳酸钙、碳酸钡与盐酸的反应可知,碳酸锶与盐酸反应生成氯化锶、水、二氧化碳.碳酸锶不溶于水,氯化锶易溶于水;
(2)①②加入少量30% H2O2溶液目的是除去亚铁离子,反应要在酸性溶液中进行;
③调节pH除去Fe3+等,不能引入杂质;
(3)①氯化锶晶体在氯化锶饱和溶液中的溶解度较小;
②由题中信息可知,当高于61℃时晶体会失去结晶水,故热风吹干六水氯化锶时温度应低于61℃;
(5)根据题中信息,硫酸锶能生成碳酸锶,说明碳酸锶的溶解度小于硫酸锶,根据元素守恒和电荷守恒书写反应的离子方程式.
解答 解:(1)碳酸锶与盐酸反应生成氯化锶、水、二氧化碳.碳酸锶不溶于水,氯化锶易溶于水.反应离子方程式为:SrCO3+2H+═Sr2++H2O+CO2↑,
故答案为:SrCO3+2H+═Sr2++H2O+CO2↑;
(2)加入少量30% H2O2溶液目的是除去亚铁离子,反应要在酸性条件下进行,所以
①A溶液的溶质是H2SO4,
故答案为:H2SO4;
②30% H2O2溶液能将Fe2+氧化到Fe3+,
故答案为:使Fe2+氧化到Fe3+;
③调节pH除去Fe3+等,要不能引入杂质,最好选用氢氧化锶粉末或氧化锶粉末;
故答案为:BD;
(3)①氯化锶晶体在氯化锶饱和溶液中的溶解度较小,洗涤氯化锶晶体选用氯化锶饱和溶液,既溶解晶体表面附着的杂质,又减少洗涤时氯化锶因溶解造成的损失,
故答案为:既溶解晶体表面附着的杂质,又减少洗涤时氯化锶因溶解造成的损失;
②由题中信息可知,当高于61℃时晶体会失去结晶水,故热风吹干六水氯化锶时温度应低于61℃,
故答案为:A;
(4)工天青石(主要成分为硫酸锶,含不溶性杂质)与碳酸钠溶液的混合物在90℃时加热1~2h,经过滤、洗涤,得到碳酸锶,根据元素守恒和电荷守恒可知该反应的离子方程式为SrSO4+CO32-=SrCO3+SO42-,
故答案为:SrSO4+CO32-=SrCO3+SO42-.
点评 本题以氯化锶的制备为载体,考查学生对工艺流程的理解、元素周期律、物质的分离提纯、沉淀转化等,综合性较强,涉及的知识点多,难度中等,需要学生具备阅读分析能力和灵活运用知识的解决问题能力.


科目:高中化学 来源: 题型:选择题
| A. | A、E一定在不同周期 | |
| B. | D在第二周期 | |
| C. | A、D可能在同一主族 | |
| D. | C、D的单质可能化合形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽油和水,四氯化碳和水 | B. | 汽油和水,苯和水 | ||
| C. | 食用油和水,醋酸和水 | D. | 葡萄糖和水,酒精和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 Ⅱ
Ⅱ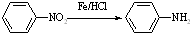 (苯胺,易被氧化)
(苯胺,易被氧化) ;
; +2NaOH→
+2NaOH→ +HCOONa+H2O.
+HCOONa+H2O.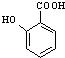 有多种同分异构体,其中含符合下列条件的共有2种.
有多种同分异构体,其中含符合下列条件的共有2种. 的过程.
的过程.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 量取10mL该溶液倒入试管中,试管中,试管中Na+的物质的量为0.08mol | |
| B. | 该溶液的物质的量浓度为0.8mol•L-1 | |
| C. | 该溶液中含有46.8g NaCl | |
| D. | 配置50mL该溶液需用23.4g NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,可使①②③④反应速率均加快 | |
| B. | △H3=-110.5kJ.mol-1,△H4=+172.5kJ.mol-1 | |
| C. | 反应①②③④均属于化合反应、氧化还原反应 | |
| D. | CO的燃烧热是566.0kJ.mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com