
【题目】下图为两个原电池装置图,由此判断下列说法错误的是( )

A.当两电池转移相同电子时,生成和消耗Ni的物质的量相同
B.两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动
C.由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应
D.由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn
科目:高中化学 来源: 题型:
【题目】
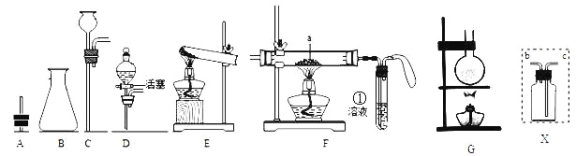
(1)用上图仪器组装成气体发生装置:制取O2可选的装置是______________。
(2)若用装置X收集制取的O2,瓶中装满水,氧气应从_____________端通入。
(3)若用F装置进行CO还原CuO的实验,实验室制取CO的方法可采取甲酸脱水法(HCOOH![]() CO↑+H2O),用纯净的CO完成该实验。
CO↑+H2O),用纯净的CO完成该实验。
I.除F、X外还需要的装置有______________,X中应加入的试剂是_________。
II.实验时①处选择的溶液可以为_______,其作用是_____________;F装置中气球的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1.43 g Na2CO3·xH2O溶于水配成10 mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0 mL,并收集到112 mL CO2(标准状况)。试计算:
⑴CO2的物质的量
⑵Na2CO3·xH2O的物质的量。
⑶x的值。
⑷所用稀盐酸的物质的浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0
4NO2(g)+O2(g) ΔH>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将________(填“增大”、“减小”或“不变”)。
②下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1 000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为__________。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2________T1。
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的________区生成,其电极反应式为______________
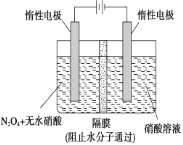
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g·cm-1)配制为1mol·L-1的稀硫酸100ml。
(1)选用的主要仪器有:
①玻璃棒,②_________,③胶头滴管,④量筒,⑤__________。
(2)需要用量筒量取98%的浓硫酸________ml。
(3)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗净2~3次并转入容量瓶
E.稀释浓H2SO4
F.将溶液转入容量瓶
其操作正确的顺序依次为_____________________。
(4)简要回答下列问题:
①如果实验室有10mL、20mL、50mL的量筒,则所需的浓硫酸应选用____________mL的量筒最好
②任何实验都有误差,下列哪些操作会使所配的溶液浓度偏大____________
A.配置前,量取浓硫酸时发现量筒不干净用水洗净后直接量取
B.将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌,若搅拌过程中有液体溅出
C.在转入容量瓶前烧杯中液体未冷却至室温
D.洗涤烧杯和玻璃棒2~3次,洗涤液未转入容量瓶
E.定容时俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O![]() Al2O3+3H2,电解过程中,以下判断正确的是( )
Al2O3+3H2,电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e═Pb2++2H2O | 阳极:2Al+3H2O6e═Al2O3+6H+ |
D |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为____________mol
(2)该气体所含原子总数为____________个。
(3)该气体在标准状况下的体积为__________L
(4)该气体溶于1ml水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为_________mol· L-1。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)
2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量__________,密度___________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时减小一倍,平衡将向__________移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_______________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将______________(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_____________(填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com