
| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | FeS2 | S | Na2S2O3 | SO3或H2SO4或Na2SO4 | Na2S2O8 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
 根据废水中所含有害物质的不同,工业上有多种废水的处理方法.
根据废水中所含有害物质的不同,工业上有多种废水的处理方法.| 8000×(15-cV2) |
| V1 |
| 8000×(15-cV2) |
| V1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | Na2S等 Na2S等 |
FeS2 | S | Na2S2O3 | SO2等 SO2等 |
SO3或H2SO4或Na2SO4 | Na2S2O8 |
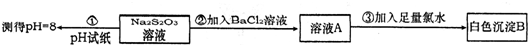
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 8000×(15-cV2) |
| V1 |
| 8000×(15-cV2) |
| V1 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年重庆市高三上学期12月月考理综化学试卷(解析版) 题型:填空题
硫元素有多种化合价,可形成多种化合物。
(1)常温下用1 mol·L﹣1 100 mL NaOH溶液恰好完全吸收0.1 mol SO2气体,此反应的离子方程式为 ;该溶液pH_______7(填“=”“>”或“<”)。
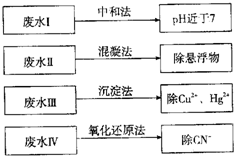
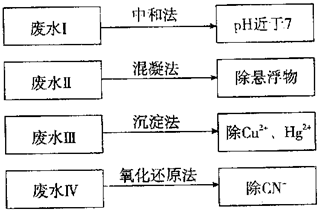
(2)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。

实验①可说明________(填字母)
A.该Na2S2O3溶液中水电离的c(OH﹣)=10﹣8mol/L
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3水解方程式为S2O32﹣+2H2O=H2S2O3+2OH﹣
写出实验②发生反应的离子方程式 。
(3)实验室制得的Na2S2O3粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O(摩尔质量为248g/mol)的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。称取1.28 g的粗样品溶于水,用0.40mol/L KMnO4溶液(加入适量硫酸酸化)滴定,当溶液中S2O32﹣全部被氧化时,消耗KMnO4溶液体积20.00 mL。(已知:5S2O32﹣+8MnO4﹣+14H+=8Mn2++10SO42﹣+7H2O)。
试回答:
①KMnO4溶液置于——(填“酸式”或“碱式”)滴定管中,滴定终点的现象为 。
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果_____________(填“偏高”“偏低”或“不变”)。
③产品中Na2S2O3·5H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省福州市毕业班质量检查理综化学试卷(解析版) 题型:选择题
不锈钢的种类很多,其中一种铁元素以外,还含有较多的Cr(铬)、Ni(镍)、Mo(钼),少量 的Si(硅)、C(碳),微量的S(硫)、P(磷)。
(1)上述元素中属于第三周期且第一电离能从大到小排列的是_______
(2)Mo(钼)处于第五周期,且与Cr(铬)元素位于同一族,则基态Mo(钼)原子的外围电子(价电子)排布式是_______。
(3)CH4的沸点比SiH4低,原因是_______。
(4)镍元素能形成多种配合物,配离子[Ni(CN)4]2—中不含有的是____(填选项编号)。
A.离子键 B.配位键 C.σ键 D.π键 E.氢键
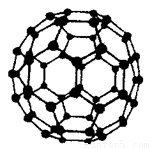
(5)碳元素有多种单质,其中C60分子有独特的球形结构:C60分子中原子轨道杂化类型是_______。
(6)碳的另一种单质石墨呈层状结构,有一碳镁新型材料就是在石墨碳原子层间加人镁原子层,两层俯视图:
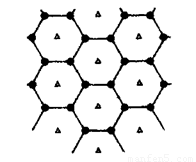
该材料的化学式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com