
| A. | 碘的CCl4溶液呈紫红色 | |
| B. | 碘在CCl4中的溶解度比在水中的溶解度大 | |
| C. | 萃取时,要充分振荡混合液体并适当旋转活塞排气减压 | |
| D. | 分液时,水从分液漏斗下口流出,碘的CCl4溶液从漏斗上口倒出 |
分析 碘在CCl4中的溶解度比在水中的溶解度大,可用四氯化碳萃取,萃取时,要检查分液漏斗是否漏液,充分振荡混合液体并适当旋转活塞排气减压,分液时,水从分液漏斗上口流出,碘的CCl4溶液从漏斗下口流出,以此解答该题.
解答 解:A.碘易溶于四氯化碳,CCl4溶液呈紫红色,故A错误;
B.碘在CCl4中的溶解度比在水中的溶解度大,可用四氯化碳萃取,故B正确;
C.振荡混合液体易使分液漏斗内压强过大,应适当旋转活塞排气减压,故C正确;
D.分液时,水从分液漏斗上口流出,碘的CCl4溶液从漏斗下口流出,易避免重新混合而污染,故D错误.
故选D.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意基础知识的巩固,注意相关化学实验的基本操作方法.


科目:高中化学 来源: 题型:选择题
| A. | 把浑浊的液体倒入蒸发皿内加热 | |
| B. | 开始析出晶体后用玻璃棒搅拌 | |
| C. | 加入试剂的顺序为Na2CO3、BaCl2、NaOH、HCl | |
| D. | 用过滤法除去粗盐中的泥沙 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
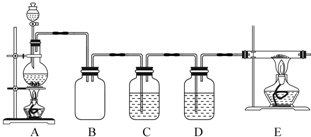
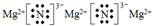 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧热是101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量 | |
| B. | 工业上用点燃H2、Cl2混合气体的方法生产盐酸 | |
| C. | 金属钠着火时可用干燥的沙土来灭火 | |
| D. | 驰名世界的中国瓷器是硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量 | |
| B. | O2前面的$\frac{1}{2}$表示参加反应的O2的分子数目 | |
| C. | 燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ•mol-1 | |
| D. | 1 mol H2和$\frac{1}{2}$ mol O2所具有的总能量大于1mol H2O(g)所具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
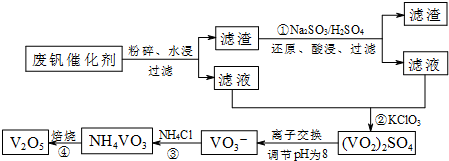
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com