
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | 只有⑤ |
分析 ①该离子方程式表示可溶性碳酸盐和强酸反应;
②该离子方程式表示强酸与强碱的反应;
③该离子方程式表示硝酸银与盐酸或可溶性氯化物的反应;
④该反应表示铁与可溶性铜盐的反应;
⑤该反应只能表示水与氯气的反应.
解答 解:①CO32-+2H+═CO2↑+H2O为可溶性碳酸盐和强酸的一类反应,如碳酸钠与盐酸、碳酸钾与硫酸等,故①错误;
②OH-+H+═H2O为强酸与强碱的反应生成可溶性盐和水的一类反应,如盐酸与NaOH、硫酸与KOH等,故②错误;
③Ag++Cl-═AgCl↓表示硝酸银与可溶性氯化物的一类反应,如硝酸银与氯化钠、盐酸、氯化钾等,故③错误;
④Fe+Cu2+═Fe2++Cu表示Fe与可溶性铜盐的反应,如铁与硝酸铜、硫酸铜、氯化铜等,故④错误;
⑤Cl2+H2O═H++Cl-+HClO只能表示氯气与水的反应,满足条件,故⑤正确;
故选D.
点评 本题考查了离子方程式的书写方法及表示意义,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式表示的意义,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LNaOH溶液中:Na+、K+、Ca2+、HCO3- | |
| B. | 无色溶液中:H+、Fe2+、Al3+、NO3- | |
| C. | 与铝产生氢气的溶液中:NH4+、Cl-、Mg2+、SO42- | |
| D. | pH>7的溶液中:Na+、K+、AlO2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液可保存在玻璃塞的试剂瓶中 | |
| B. | 液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 | |
| C. | 配制500ml 0.1mol/L的NaOH溶液时,应用托盘天平称取2.00g NaOH固体 | |
| D. | 氢氟酸可保存在棕色玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 盛放烧碱溶液的试剂瓶不能用玻璃塞,是因为:SiO2+2OH-═SiO32-+H2O | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水保存在棕色细口瓶中 | B. | NaOH保存在具有玻璃塞的细口瓶中 | ||
| C. | 金属钠保存在CCl4中 | D. | 氢氟酸保存在玻璃塞的细口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
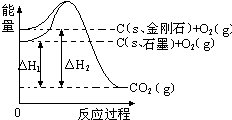 如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )| A. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 石墨和金刚石是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com