


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氧化物 氧化铁 FeO |
| B、盐 纯碱 Na2CO3 |
| C、酸 硫酸 H2S |
| D、酸性氧化物 碳酸气 C0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
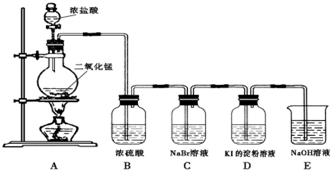
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | (1) | (2) | (3) | (4) | (5) |
| 操作 | a+b | a+e | b+c | b+d | d+f |
| 反应 现象 | 产生白色 沉淀 | 有无色气体 产生 | 产生白色 沉淀 | 产生白色 沉淀 | 溶液呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol某粒子集体所含该粒子数与0.012kg12C中所含碳原子数相同 |
| B、1mol任何粒子的粒子数叫做阿伏加德罗常数,通常表示为6.02×1023mol-1 |
| C、O22-的摩尔质量为34g/mol |
| D、常温常压下28g N2所含分子数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
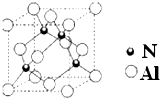 【选做题--物质结构与性质】
【选做题--物质结构与性质】查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com