
| A. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| B. | 给试管里的液体加热,液体的体积一般不超过试管容积的$\frac{2}{3}$ | |
| C. | 酒精着火时可用水扑灭 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
分析 A、根据酸、碱的性质分析,酸、碱都具有腐蚀性,但相对来讲,酸性、碱性越弱,腐蚀性越弱;
B、试管内液体过多,加热时容易溅出伤人;
C、酒精能与水任意比互溶;
D、量筒不能受热.
解答 解:A、碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,不能用硫酸或盐酸冲洗,硫酸和盐酸也有腐蚀性,会造成二次伤害,故A正确;
B、试管内液体过多,加热时容易溅出伤人,故一般不超过试管容积的$\frac{1}{3}$,故B错误;
C、酒精能与水任意比互溶,故当酒精着火时,如果用水灭,不但不能灭火,还会增大着火面积,应用湿抹布盖灭,故C错误;
D、量筒不能受热,故浓硫酸的稀释不能在量筒中进行,故D错误.
故选A.
点评 本题考查了实验室的常见的操作正误的判断以及危险的处理,难度不大,应注意的是酒精着火不能用水灭,应用湿抹布盖灭.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 2:3 | C. | 1:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢能可再生,没有污染,现已用作火箭和燃料电池的燃料 | |
| B. | 在环保领域,酸性或碱性废水的处理常常利用中和反应 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 工业生产中,使用催化剂能加快化学反应速率,提高反应物的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中 Fe2+是还原剂,O2 是还原产物 | |
| B. | 4molNa2O2 在反应中共得到 8NA 的电子 | |
| C. | Fe(OH)3既是氧化产物又是还原产物,每生成 4mol Fe(OH)3 反应过程中共转移电子 6mol | |
| D. | 反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | NO2 | C. | NO | D. | N2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  证明非金属性强弱S>C>Si | |
| B. |  制备并收集少量NO气体 | |
| C. |  制取并收集干燥纯净的NH3 | |
| D. |  制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电解过程中,a 电极表面先有红色物质析出,后有气泡产生 | |
| B. | b 电极上发生反应的方程式为:4OH--4e-=2H2O+O2↑ | |
| C. | 曲线 O~P 段表示 O2 的体积变化 | |
| D. | 从开始到 Q 点时收集到的混合气体的平均摩尔质量为 12 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
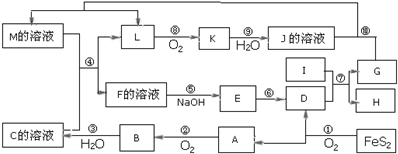
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com