
某同学进行试验探究时,欲配制1.0mol•L﹣1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2•8H2O试剂(化学式量:315).在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物.为探究原因,该同学查得Ba(OH)2•8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6.
(1)烧杯中未溶物仅为BaCO3,理由是
(2)假设试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. |
|
| 步骤2:取适量滤液于试管中,滴加稀硫酸. |
|
| 步骤3:取适量步骤1中的沉淀于是试管中, |
|
| 步骤4: |
|
(3)将试剂初步提纯后,准确测定其中Ba(OH)2•8H2O的含量.实验如下:
①配制250ml 约0.1mol•L﹣1Ba(OH)2•8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水, ,将溶液转入 ,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将
(填“0.020”、“0.05”、“0.1980”或“1.5”)mol•L﹣1盐酸装入50ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.
(4)室温下, (填“能”或“不能”) 配制1.0mol•L﹣1Ba(OH)2溶液.
考点:
配制一定物质的量浓度的溶液.
专题:
实验题.
分析:
(1)Ba(OH)2•8H2O与CO2作用转化为BaCO3;
(2)步骤2:预期现象和结论:有白色沉淀生成,说明有Ba2+;
步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中.
预期现象和结论:试管中有气泡生成,烧杯中的澄清石灰水变浑浊,结合步骤2说明沉淀是BaCO3;
步骤4:取适量滤液于烧杯中,用pH计测其pH值;
预期现象和结论:pH>9.6,说明有大量的OH﹣,综合上面步骤可知试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,假设成立,
(3)①将样品在烧杯中溶解后,将溶液移入250mL容量瓶中,洗涤将洗涤液移入容量瓶,定容、摇匀;
②盐酸体积最多不能多于50ml,根据50mL计算盐酸的最小浓度,应该是选大于最小浓度而且接近的;
(4)根据氢氧化钡的溶解度估算饱和溶液的物质的量浓度,据此判断
解答:
解:(1)烧杯中未溶物仅为BaCO3,则由于Ba(OH)2•8H2O与CO2作用转化为BaCO3,
故答案为:Ba(OH)2•8H2O与CO2作用转化为BaCO3;
(2)
步骤2:由于BaCO3能和稀硫酸反应生成二氧化碳和硫酸钡沉淀,故预期现象和结论:有白色沉淀生成,说明有Ba2+;
步骤3:取适量步骤1中的沉淀于试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中,BaCO3能和盐酸反应生成的二氧化碳气体能使石灰水变浑浊,故预期现象和结论:试管中有气泡生成,烧杯中的澄清石灰水变浑浊,结合步骤2说明沉淀是BaCO3;
步骤4:取适量滤液于烧杯中,用pH计测其pH值.预期现象和结论:pH>9.6,说明有大量的OH﹣,综合上面步骤可知试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,假设成立,
故答案为:步骤2:预期现象和结论:有白色沉淀生成,说明有Ba2+;
步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中;
预期现象和结论:试管中有气泡生成,烧杯中的澄清石灰水变浑浊,结合步骤2说明沉淀是BaCO3;
步骤4:取适量滤液于烧杯中,用pH计测其pH值;
预期现象和结论:pH>9.6,说明有大量的OH﹣,综合上面步骤可知试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,假设成立;
(3)①将样品在烧杯中溶解并过滤除去碳酸钙后后,将溶液移入250mL容量瓶中,洗涤将洗涤液移入容量瓶,定容、摇匀,
故答案为:溶解、过滤;250ml的容量瓶中;
②盐酸体积最多不能多于50ml,根据50mL计算盐酸的最小浓度,令盐酸的最小浓度为amol/L,则:
0.025L×0.1mol/L×2=amol/L×0.05L,解得a=0.1mol/L,应该是选大于最小浓度而且接近的,故选择0.1980mol/L的盐酸,
故答案为:0.1980;
(4)室温下,氢氧化钡的溶解度为3.9g,溶液的物质的量浓度约是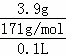 =0.23mol/L,故室温下,不能配制1.0mol•L﹣1Ba(OH)2溶液,
=0.23mol/L,故室温下,不能配制1.0mol•L﹣1Ba(OH)2溶液,
故答案为:不能.
点评:
本题考查物质成分与含量测定、对实验方案的理解与设计、溶液配制、中和滴定、化学计算等,题目综合性较大,难度中等,侧重对实验方案设计与化学计算,是对学生综合能力的考查.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
有关碰撞理论,下列说法中不正确的是( )
A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应
B.增大反应物浓度,单位体积内活化分子数增多,有效碰撞几率增大,反应速率增大
C.升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大
D.正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是( )
A. 物质的量之比为1:1 B. 物质的量之比为1:2
C. 质量之比为4:1 D. 质量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
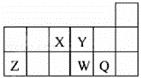
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )
|
| A. | 元素X与元素Z的最高正化合价之和的数值等于8 |
|
| B. | 原子半径的大小顺序为:rX>rY>rZ>rW>rQ |
|
| C. | 离子Y2﹣和Z3+的核外电子数和电子层数都不相同 |
|
| D. | 元素W的最高价氧化物对应的水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,将1.000mol•L﹣1盐酸滴入20.00mL 1.000mol•L﹣1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )

|
| A. | a点由水电离出的c(H+)=1.0×10﹣14mol•L﹣1 |
|
| B. | b点:c(NH4+)+c(NH3•H2O)=c(Cl﹣) |
|
| C. | c点:c(Cl﹣)=c(NH4+) |
|
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质与应用均正确的是
A.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
B.乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同
C.Mg(OH)2难溶于水,但可缓慢溶于浓的NH4Cl溶液
D.油脂在酸性条件下可以水解,可用此反应可以制作肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、A、B、C在元素周期表的位置如右图所示,A是电负性最大的元素,则下列说法不正确的是
| X | A | ||
| Y | C | B |
A.原子半径由小到大的顺序为:A<B<C<Y
B.A、B的氢化物的沸点由低到高的顺序为:HA<HB
C.X、Y最高价氧化物对应的水化物的酸性由弱到强的顺序为:H2YO3<H2XO3
D.B、C简单离子的还原性由弱到强的顺序为:B-<C2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com