
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H20+SO2═2NH4++SO32-+H2O | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+═2Fe3++3H2O |
分析 A.用过量氨水吸收工业尾气中的SO2,二者反应生成亚硫酸铵;
B.浓盐酸和高锰酸钾反应生成氯气;
C.用Cu作电极时电解硫酸铜溶液,该装置是电镀池,阳极上Cu失电子发生氧化反应;
D.氧化铁和氢离子反应生成铁离子,铁离子和碘离子反应生成碘单质和亚铁离子.
解答 解:A.用过量氨水吸收工业尾气中的SO2,二者反应生成亚硫酸铵,离子方程式为2NH3•H20+SO2═2NH4++SO32-+H2O,故A正确;
B.浓盐酸可以被酸性高锰酸钾溶液氧化,从而影响双氧水还原性的检验,故B错误;
C.用Cu作电极时电解硫酸铜溶液,该装置是电镀池,阳极上Cu失电子发生氧化反应,阳极反应式为Cu-2e-=Cu2+,阴极反应式为Cu2++2e-=Cu,故C错误;
D.氧化铁和氢离子反应生成铁离子,铁离子和碘离子反应生成碘单质和亚铁离子,离子方程式为Fe2O3+6H++2I-═2Fe2++3H2O+I2,故D错误;
故选A.
点评 本题考查离子方程式正误判断,为高频考点,明确离子方程式书写规则、物质性质是解本题关键,涉及氧化还原反应、复分解反应,易错选项是D,注意铁离子和碘离子发生的氧化还原反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
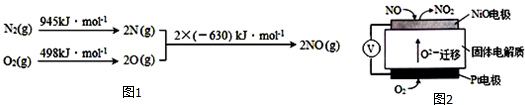
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液体均一,呈紫红色 | |
| B. | 液体分两层,上层为紫红色,下层为无色 | |
| C. | 液体分两层,上层为无色,下层为紫红色 | |
| D. | 液体均一,呈无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
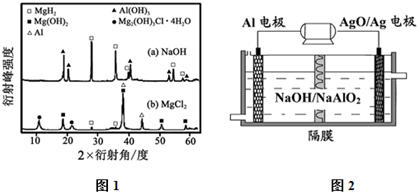
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
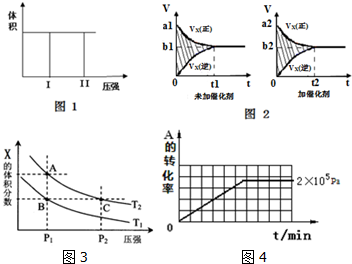
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
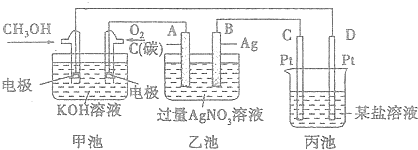
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物平衡浓度较大 | B. | 反应越有利于往逆反应方向进行 | ||
| C. | 反应进行的越彻底 | D. | 生成物平衡浓度较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{100w}{w+18a}$% | B. | $\frac{7100w}{161(w+18a)}$% | C. | $\frac{100w}{w+36a}$% | D. | $\frac{7100w}{161(w+36a)}$% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一氧化碳的转化率提高,水蒸气的转化率降低 | |
| B. | 反应物的转化率都提高 | |
| C. | 平衡向正反应方向移动,达到新的平衡时二氧化碳的体积分数增大 | |
| D. | 平衡向正反应方向移动,二氧化碳的物质的量将大于1 mol但小于2 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com