


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省五校协作体高三上学期期初考试化学试卷(解析版) 题型:选择题
某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g)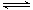 H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
A.升高温度 B.加入催化剂
C.再加入n molCO和n molH2O D.再加入2n molCO2和2n molH2
查看答案和解析>>
科目:高中化学 来源:2010年浙江江山实验中学高二年级5月月考化学试卷 题型:选择题
某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g)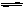 H2(g)+CO2(g)
H2(g)+CO2(g)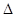 H>0当反应达平衡时,测得容器中各物质均 为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可采用的是( )
H>0当反应达平衡时,测得容器中各物质均 为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可采用的是( )
A、升温 B、加催化剂
C、再加入n molCO和n molH2O D、再加入2n molCO2和2n molH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com