

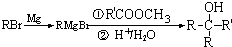 ②
②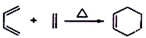
 .
. .
.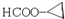 .
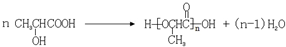
.分析 5.4g水的物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为$\frac{13.2g}{44g/mol}$=0.3mol,n(C)=n(CO2)=0.3 mol,9gA的物质的量为$\frac{9g}{90g/mol}$=0.1mol,故A分子中N(C)=$\frac{0.3mol}{0.1mol}$=3、N(H)=$\frac{0.6mol}{0.1mol}$=6,则分子中N(O)=$\frac{90-12×3-6}{16}$=3,故有机物A为C3H6O3,1molA与Na反应生成1molH2、与NaHCO3反应生成1molCO2,则A含有一个羟基、一个羧基,核磁共振氢谱图中有4个吸收峰,且面积比为3:1:1:1,则A的结构简式为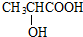 .A发生消去反应生成B为CH2=CHCOOH,B与甲醇发生酯化反应生成C为CH2=CHCOOCH3,C与异戊二烯发生加成反应生成D为
.A发生消去反应生成B为CH2=CHCOOH,B与甲醇发生酯化反应生成C为CH2=CHCOOCH3,C与异戊二烯发生加成反应生成D为 .葡萄糖在酒化酶作用下得到CH3CH2OH,乙醇与氢溴酸发生取代反应得到E为CH3CH2Br,溴乙烷与Mg反应得到F为CH3CH2MgBr,F与D反应生成X.
.葡萄糖在酒化酶作用下得到CH3CH2OH,乙醇与氢溴酸发生取代反应得到E为CH3CH2Br,溴乙烷与Mg反应得到F为CH3CH2MgBr,F与D反应生成X.
解答 解:5.4g水的物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为$\frac{13.2g}{44g/mol}$=0.3mol,n(C)=n(CO2)=0.3 mol,9gA的物质的量为$\frac{9g}{90g/mol}$=0.1mol,故A分子中N(C)=$\frac{0.3mol}{0.1mol}$=3、N(H)=$\frac{0.6mol}{0.1mol}$=6,则分子中N(O)=$\frac{90-12×3-6}{16}$=3,故有机物A为C3H6O3,1molA与Na反应生成1molH2、与NaHCO3反应生成1molCO2,则A含有一个羟基、一个羧基,核磁共振氢谱图中有4个吸收峰,且面积比为3:1:1:1,则A的结构简式为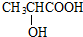 .A发生消去反应生成B为CH2=CHCOOH,B与甲醇发生酯化反应生成C为CH2=CHCOOCH3,C与异戊二烯发生加成反应生成D为
.A发生消去反应生成B为CH2=CHCOOH,B与甲醇发生酯化反应生成C为CH2=CHCOOCH3,C与异戊二烯发生加成反应生成D为 .葡萄糖在酒化酶作用下得到CH3CH2OH,乙醇与氢溴酸发生取代反应得到E为CH3CH2Br,溴乙烷与Mg反应得到F为CH3CH2MgBr,F与D反应生成X.
.葡萄糖在酒化酶作用下得到CH3CH2OH,乙醇与氢溴酸发生取代反应得到E为CH3CH2Br,溴乙烷与Mg反应得到F为CH3CH2MgBr,F与D反应生成X.
(1)A的分子式为:C3H6O3,A→B的反应类型为消去反应,故答案为:C3H6O3;消去反应;
(2)D的结构简式为 ,故答案为:
,故答案为: ;
;
(3)C2H6O→E转化的化学方程式:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O,
故答案为:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O;
(4)一定条件下A(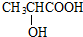 )能合成一种可降解高分子材料M,该反应方程式为:
)能合成一种可降解高分子材料M,该反应方程式为: ,
,
故答案为: ;
;
(5)符合下列条件的C(CH2=CHCOOCH3)的同分异构体:①能发生水解反应,说明含有酯基,②能发生银镜反应,为甲酸形成的酯,有HCOOCH=CHCH3、HCOOCH2CH=CH2、HCOOC(CH3)=CH2、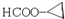 ,其中不能使溴水褪色的结构简式为:
,其中不能使溴水褪色的结构简式为: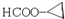 ,
,
故答案为:4;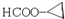 .
.
点评 本题考查有机物的推断与合成,关键是计算确定A的分子式,熟练掌握官能团的性质与转化,理解烯烃与二烯烃的加成反应,(5)中同分异构体书写为易错点,学生容易忽略环状结构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | CH3CHO+H2$→_{△}^{催化剂}$CH3CH2OH | |
| B. | 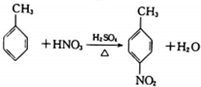 | |
| C. | 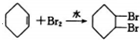 | |
| D. | 2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
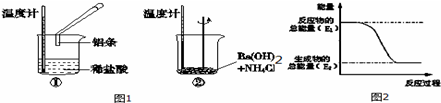
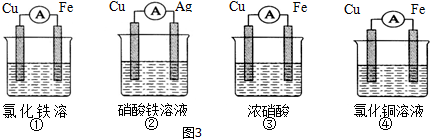
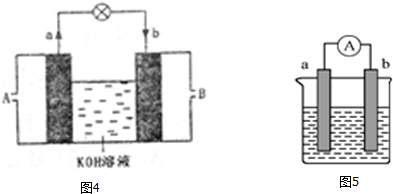
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氘(D)原子核外有2个电子 | B. | 1H与D互称同位素 | ||
| C. | H2与D2互称同素异形体 | D. | 18g D2O的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
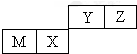
| A. | 离子半径Z<Y<M | |
| B. | X的氧化物能与水反应生成相应的酸 | |
| C. | 气态氢化物的稳定性:Z>Y>X | |
| D. | Y的最高价氧化物对应的水化物属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
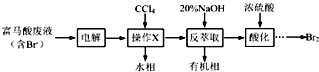

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
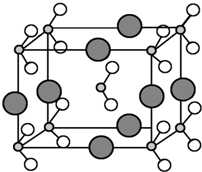 原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29.
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )
青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com