
����Ŀ��������Ԫ��Q��R��T��W��Ԫ�����ڱ���λ����ͼ��ʾ������T��������������������������ȣ� ��ش��������⣺
��1��T��ԭ�ӽṹʾ��ͼΪ �� R������⻯��ĵ���ʽΪ �� Q��1��1���⻯������Է���������С�ķ������ͷ��ӣ����幹�ͣ���
��2��Ԫ�صķǽ�����Ϊ��ԭ�ӵĵõ�����������QW���ǿ�ڡ������ڡ�����
��3��W�ĵ�����������������ˮ����Ũ��Һ�����ܷ�����Ӧ�������������ʣ�����һ�������壬��Ӧ�Ļ�ѧ����ʽΪ ��
��4��R�ж���������������������Է���������С����һ�������£�2L�ļ�������0.5L���������ϣ����û�����屻������NaOH��Һ��ȫ���պ�û����������������ɵ�R�ĺ������εĻ�ѧʽ�� ��
���𰸡�
��1��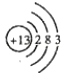 ��
��![]() ��ֱ��
��ֱ��
��2������
��3��S+2H2SO4��Ũ�� ![]() 3SO2+2H2O
3SO2+2H2O
��4��NaNO2
���������⣺�ɶ�����Ԫ��Q��R��T��W������λ�ã���ȷ��T��WΪ�������ڵ�Ԫ�أ�Q��RΪ�ڶ�����Ԫ�أ�T������������������������ȣ���TΪAlԪ�أ���QΪCԪ�أ�RΪNԪ�أ�WΪSԪ�أ���1��T��ΪAl��ԭ�Ӻ�����3�����Ӳ㣬���������Ϊ2��8��3��Al��ԭ�ӽṹʾ��ͼΪ 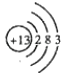 ��R������⻯��Ϊ�����������ʽΪ
��R������⻯��Ϊ�����������ʽΪ ![]() ��Q��1��1���⻯������Է���������С�ķ���ΪCH��CH��CΪsp�ӻ���Ϊֱ�߷��ӣ����Դ��ǣ�
��Q��1��1���⻯������Է���������С�ķ���ΪCH��CH��CΪsp�ӻ���Ϊֱ�߷��ӣ����Դ��ǣ�  ��
�� ![]() ��ֱ�ߣ���2����������Դ���̼������ԣ��ɱȽϷǽ�����Q��W�����Դ��ǣ����ڣ���3��WΪS��������������ˮ����Ũ��ҺΪŨ���ᣬ���߷�Ӧ���ɶ��������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪS+2H2SO4��Ũ��
��ֱ�ߣ���2����������Դ���̼������ԣ��ɱȽϷǽ�����Q��W�����Դ��ǣ����ڣ���3��WΪS��������������ˮ����Ũ��ҺΪŨ���ᣬ���߷�Ӧ���ɶ��������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪS+2H2SO4��Ũ�� ![]() 3SO2+2H2O�� ���Դ��ǣ�S+2H2SO4��Ũ��
3SO2+2H2O�� ���Դ��ǣ�S+2H2SO4��Ũ�� ![]() 3SO2+2H2O����4��RΪNԪ�أ��ж�����������м���Է���������С�����ΪNO����һ�������£�2L�ļ�������0.5L���������ϣ����û�����屻������NaOH��Һ��ȫ���պ�û�����������������������NԪ�ػ��ϼ�Ϊa�����ݵ���ת���غ㣺2��a��2��=0.5��4�����a=3�������ɵ�R�ĺ������εĻ�ѧʽ��NaNO2 �� ���Դ��ǣ�NaNO2 ��
3SO2+2H2O����4��RΪNԪ�أ��ж�����������м���Է���������С�����ΪNO����һ�������£�2L�ļ�������0.5L���������ϣ����û�����屻������NaOH��Һ��ȫ���պ�û�����������������������NԪ�ػ��ϼ�Ϊa�����ݵ���ת���غ㣺2��a��2��=0.5��4�����a=3�������ɵ�R�ĺ������εĻ�ѧʽ��NaNO2 �� ���Դ��ǣ�NaNO2 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ס��ҡ���������������ѧ��ѧ�г���������,��ת����ϵ��ͼ��ʾ����Ͷ���������
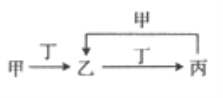
A. N2��O2 B. Cl2��Fe C. C��O2 D. SO2��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 L 1 mol��L��1 Na2SO4��Һ�У����и�����ȷ����
A��c(Na��)��1 mol��L��1 B��n(Na��)��3 mol
C��c(SO42-)��2 mol��L��1 D��m(Na2SO4)��142 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��Ϊ������Ԫ�أ����������ڱ��е�λ������ͼ����֪B��C��Ԫ�������ڱ���������֮����AԪ����������2����B��CԪ�ص�ԭ������֮����AԪ��ԭ��������4������A��B��C ���ڵ�һ���ǣ� �� 
A.Be��Na��Al
B.B��Mg��Si
C.O��P��Cl
D.C��Al��P
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���Ľ̲ĵ�֪����ͨп�̵��Ͳ����������Ҫ�ɷ�ΪMnO2��NH4Cl��ZnCl2�����ʡ�����̽���ϸɵ���ڵĺ�ɫ�����������ʱ��������ͼ��ʾʵ�飺�����й�ʵ��������У�����ȷ����

A. �������в������������Ǽӿ�����ܽ��ٶ�
B. �������IJ��������ǹ���
C. ��������ʢ��ҩƷ������������
D. ��������Ŀ���dz�ȥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���Ԫ����������ѧϰ���о�������ʵ���ж��зdz���Ҫ�����á��±���Ԫ�����ڱ�ǰ�����ڵ�һ���֣��г��ˢ���������Ԫ�������ڱ��е�λ�á�
�� | �� | �� | |||
�� | �� | �� | �� |
��ش�
��1����������Ԫ�ص�����Ϊ______
��2������Ԫ���У��ǽ�������ǿ��Ԫ����______(��Ԫ�ط���)������������ˮ����������ǿ����_______(�ѧʽ)����������ϼ���������ϼ۵Ĵ�����Ϊ4��Ԫ����_______(��Ԫ�ط���)��
��3����������������ӦԪ����ԭ�Ӱ뾶��С����______(��Ԫ�ط���)�������Ӱ뾶������______(�����ӷ���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼������ˮ����ijѧ�����������ʵ�鷽���� 
�ش��������⣺
��1���Լ�1�� �� ��������
��2���Լ�2�� �� ������ �� ���������ӷ�ӦΪ���� ���ʵ�������û�м����Լ�2��ֱ�Ӽ����Լ�3���ܷ�ʵ��ʵ��Ŀ�� �� �����ܣ���ԭ���� ��
��3����μ���ڢٲ�ʵ���ѻ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ��������������о��й㷺��Ӧ�á����������������Ͻ���ǣ� ��
A.����B.����C.�����D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��������������Ӧ�ù㷺��ij�������ú��������ķ�ͭ��Ϊԭ������������������ͼ�� 
��1��д������ʱͭ��ϡ���ᡢϡ���ᷴӦ��������ͭ�Ļ�ѧ����ʽ�� ��
��2��ȡ��������Ϊ��ȷ��Fe3+�Ƿ��������ļ��鷽���� ��
��3������c�� ��
��4������a���Ա�ѭ�����ã��û�ѧ����ʽ��ʾ����a��ѭ�����õ�ԭ��Ϊ 2NO+O2�T2NO2�� ��
��5��һ���¶��£�����ͭ���ȷֽ�����CuO��SO2���塢SO3�����O2���壬��n��SO3����n��SO2��=1��2��д������ͭ���ȷֽ�Ļ�ѧ����ʽ�� ��
��6��ijͬѧ�������ͼ��ʾ��ʵ��װ�÷ֱ�ⶨ���ɵ�SO2��SO3�����������O2����������������в�����֮������˵�����ɣ� �� 
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com