
【题目】已知在![]() 的
的![]() ,溶液中有关粒子浓度由大到小的顺序为
,溶液中有关粒子浓度由大到小的顺序为![]() 。
。
(1)该溶液中![]() ________
________![]() (填“>”“=”或“<”),简述理由:_______________________________________________________________
(填“>”“=”或“<”),简述理由:_______________________________________________________________
(2)现向![]() 溶液中,逐滴加入少量含有酚酞的
溶液中,逐滴加入少量含有酚酞的![]() 溶液,可观察到的现象是__________________________________________________________;写出该反应的离子方程式:____________________________________。
溶液,可观察到的现象是__________________________________________________________;写出该反应的离子方程式:____________________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL浓度14.0mol/L的硝酸中,得到NO2和N2O4的混合气体1120ml(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时得到2.54g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.NO2和N2O4的混合气体中,NO2的体积分数是80%
C.得到2.54g沉淀时加入NaOH溶液的体积是600mL
D.溶解合金消耗HNO3的量是0.12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同物质的量浓度的 HC1 溶液,分别滴定物质的量浓度均为 0.1 mol/L 的三种碱溶液,滴定 曲线如图所示。下列判断正确的是
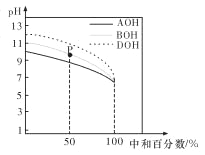
A. 滴定前,三种碱溶液中水电离出的 c(H+)大小关系: DOH>BOH>AOH
B. pH= 7 时,c(A+)=c(B+)=c(D+)
C. 滴定至 P 点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+)
D. 当中和百分数达 100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将0.1 mol/L的NaOH溶液滴入盛有50 mLpH=2 的HA溶液的绝热容器中,加入NaOH溶液的体积V与溶液温度T的关系如图。下列说法正确的是( )

A.a点溶液中,c(A-)+c(HA)=0.08 mol/L
B.b点溶液中,c(A-)<c(Na+)
C.a→b的过程中,发生了吸热反应
D.溶液中HA的电离平衡常数a点等于b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语正确的是( )
A. 氢氧根的电子式: ![]() H
H
B. 离子结构示意图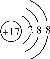 既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-
C. NH5的结构与NH4Cl相似,NH5的结构式: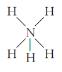
D. 丙烯的结构简式:C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比![]() 高效,且腐蚀性小。请回答下列问题:
高效,且腐蚀性小。请回答下列问题:
(1)![]() 净水的原理是________________________________________。
净水的原理是________________________________________。![]() 溶液腐蚀钢铁设备,除
溶液腐蚀钢铁设备,除![]() 作用外,另一主要原因是(用离子方程式表示)__________________________________。
作用外,另一主要原因是(用离子方程式表示)__________________________________。
(2)![]() 在溶液中分三步水解:
在溶液中分三步水解:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
以上水解反应的平衡常数![]() 由大到小的顺序是___________________________________________________________。
由大到小的顺序是___________________________________________________________。
(3)通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为:![]()
![]()
![]()
欲使平衡正向移动可采用的方法是(填序号)________。
a.降温 b.加水稀释
c.加入![]() d.加入
d.加入![]()
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是![]()
A. 如图表示同温度下,
如图表示同温度下,![]() 的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B. 如图表示
如图表示![]()
![]() 溶液滴定
溶液滴定![]()
![]()
![]() 溶液所得到的滴定曲线
溶液所得到的滴定曲线
C. 如图表示压强对可逆反应
如图表示压强对可逆反应![]() 的影响,乙的压强比甲的压强大
的影响,乙的压强比甲的压强大
D. 如图若除去
如图若除去![]() 溶液中的
溶液中的![]() 可向溶液中加入适量CuO至pH在4左右
可向溶液中加入适量CuO至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,发生反应:①M(s)+N(g) ![]() R(g) △H=—Q1 kJ/mol,②2R(g)+N(g)
R(g) △H=—Q1 kJ/mol,②2R(g)+N(g) ![]() 2T(g) △H=—Q2 kJ/mol.Q1、Q2、Q3均为正值.下列说法正确的是 ( )
2T(g) △H=—Q2 kJ/mol.Q1、Q2、Q3均为正值.下列说法正确的是 ( )
A.1mol R(g)的能量总和大于1mol M(s)与1mol N(g)的能量总和
B.将2mol R(g)与1mol N(g)在该条件下反应,可以放出热量Q2 kJ
C.当1mol M(s)完全转化为T(g)时(假定无热量损失),放出热量![]()
D.M(g)+N(g) ![]() R(g) △H=—Q3 kJ/mol,则Q3 >Q1
R(g) △H=—Q3 kJ/mol,则Q3 >Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )

A.粗盐水中含Ca2+、Mg2+、SO42-等离子,精制时除杂试剂BaCl2溶液应在Na2CO3溶液之前加入
B.标准状况下每生成22.4LCl2,便产生2 mol NaOH
C.从E口逸出的气体是Cl2
D.从B口加入含少量NaOH的水溶液以增强导电性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com