
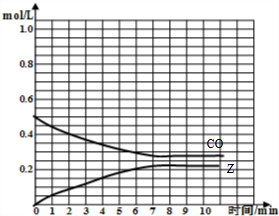
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
| 1mol |
| 2L |
| 0.55mol |
| 2L |
| 0.45mol |
| 2L |
 ,
, ;
;
| ||
| 5min-3min |


科目:高中化学 来源:不详 题型:单选题
| A.NH3的消耗速率等于NH3的生成速率 |
| B.混合气体的密度保持不变 |
| C.NO的物质的量保持不变 |
| D.NH3和O2的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.①④⑥ | C.②③⑥ | D.②③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
| ||

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验编号 | t(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | ______ | 1.20×10-3 | ______ | 124 |
| Ⅲ | 350 | ______ | ______ | 82 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

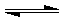
| A.若a=2,则A为液态或固体 |
| B.该反应的正反应为放热反应 |
| C.T2>T1,P2>P1 |
| D.其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
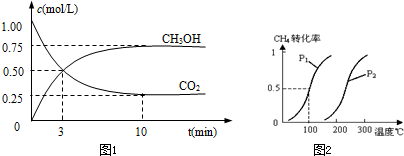
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 温度(K) CO2转化率% n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com