
| | 物质(杂质) | 除杂方法 |
| A | Cl2(HCl) | 将气体通过盛有氢氧化钠溶液的洗气瓶 |
| B | CO2(HCl) | 将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
| C | 氢氧化铁胶体 (FeCl3) | 将混合物直接过滤 |
| D | SiO2 (CaCO3) | 加入盐酸后过滤 |
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:不详 题型:单选题
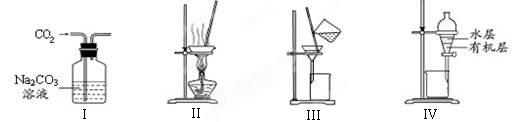
| A.用图Ⅰ所示装置除去CO2中含有的少量HCl |
| B.用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图Ⅲ所示装置分离NaCl和Na2SO4的混合溶液 |
| D.用图Ⅳ所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
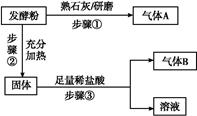
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量样品溶于足量的盐酸后,将溶液分成两份,分别装入A、B试管中 | |
| 步骤2: | ,证明有Na+,发酵粉中有NaHCO3 |
| 步骤3: | ,结合步骤2中的结论,假设2成立 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验操作 |
| A | 该物质一定是氨气 | 该物质的水溶液能使红色石蕊试纸变蓝 |
| B | 除去硫酸钠溶液中少量氯化钠杂质 | 向含有氯化钠杂质的硫酸钠溶液中加入适量的硝酸银溶液,过滤 |
| C | 该溶液一定含有大量碳酸根离子 | 某物质的水溶液中加入盐酸产生无色无味气体 |
| D | 浓硝酸的氧化性强于稀硝酸 | 向盛有少量的浓硝酸、稀硝酸的两支试管中,分别加入大小相同的铜片 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
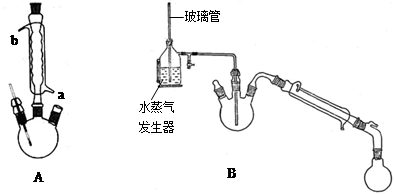
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
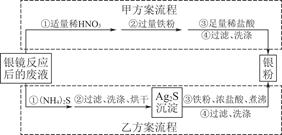
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
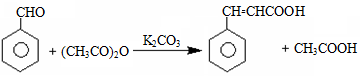
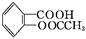 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: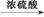
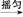
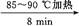
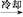
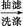 粗产品
粗产品
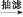
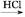
 乙酰水杨酸
乙酰水杨酸 测熔点
测熔点| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
 乙酰水杨酸
乙酰水杨酸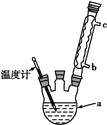
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
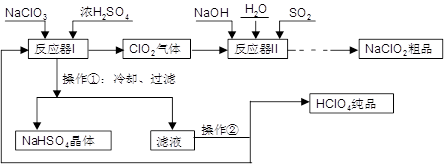
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com