
�����㶹����һ����������Ѫ�ܼ�����ҩ�����ͨ�����·����ϳɣ����ַ�Ӧ����ʡ�ԣ�
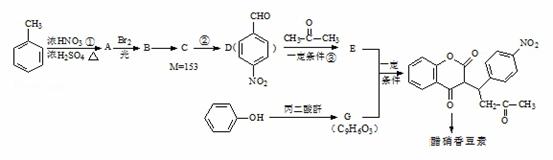
��֪��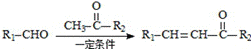 +H2O
+H2O
�ش��������⣺
��1����Ӧ�ٵķ�Ӧ������
��2��д���������ʵĽṹ��ʽ��
B G
��3����Ӧ�ڵĻ�ѧ����ʽΪ
��4����Ӧ�۵Ļ�ѧ����ʽΪ
��5������E���ʣ�����˵����ȷ���� ������ĸ��ţ���
a���ں˴Ź������������������շ� b����������ˮ��Һ����D��E
c�����Է����ӳɷ�Ӧ���ۺϷ�Ӧ��������Ӧ�ͻ�ԭ��Ӧ d������˳���칹
��6�����ӽṹ��ֻ����һ��������ͬʱ��������������G��ͬ���칹�干�� ��
�ٿ����Ȼ�����Һ������ɫ��Ӧ�� �ڿ���̼��������Һ��Ӧ���ɶ�����̼���塣
���У������ϵ�һ�ȴ���ֻ�����ֵ�ͬ���칹��Ľṹ��ʽΪ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ͼ��ʾװ��(β������������)����ȡһ����̼�������Բⶨijͭ����Ʒ(����CuO��ĩ)�н���ͭ�ĺ�����
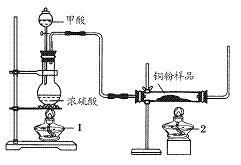
(1)�Ʊ�һ����̼�Ļ�ѧ����ʽ��___________________��
(2)ʵ���У��۲쵽��Ӧ���з�����������_____________��β������Ҫ�ɷ���_________��
(3)��Ӧ��ɺ���ȷ�IJ���˳��Ϊ________(����ĸ)
a���ر�©������ b��Ϩ��ƾ���1 c��Ϩ��ƾ���2
(4)��ʵ���г�ȡͭ����Ʒ10.0 g����ַ�Ӧ��Ӧ����ʣ����������Ϊ9.6 g����ԭ��Ʒ�е���ͭ����������Ϊ________��
(5)��Ũ���ᡢŨ���ᡢ����ˮ��˫��ˮ��ѡ�ú��ʵ��Լ������һ���ⶨ��Ʒ�н���ͭ������������ѷ�����
����Ʒ�������Ҫ������(���������������̵�ϸ��)__________��
��д���йط�Ӧ�Ļ�ѧ����ʽ��______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������������,����˵������ȷ����(C)
A. ���е���������Ǽ�
B. ��ʽ��������������Ǽ�
C. һ�����ʲ����ܼ��������Ǽ�
D. �������Ǽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȲΪ��Ҫԭ�Ͽ��Ժϳɾ�����ϩ���۱�ϩ����ȶ������Ʊ��������£�
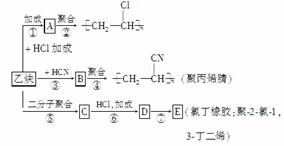
��֪��Ӧ��
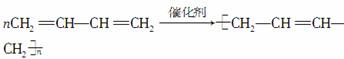
(1)��д��B��C�Ľṹ��ʽ��B______________��C______________________��
(2)д����Ӧ�ۺͷ�Ӧ�ߵĻ�ѧ����ʽ��ָ����Ӧ���͡�
________________________________________________________________________
________________________________________________________________________��
________________________________________________________________________
________________________________________________________________________��
(3)��ij�۱�ϩ���ƽ����Է�������Ϊ26 500����n��________��
(4)��������Ȳ��һ�������¿ɾۺϳɻ�״���ӣ��÷��ӵĽṹ��ʽ�ɱ�ʾΪ
______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���������
A��������Һ������������ѿ�Ǻ������� B�����顢��ȩ������ķе�������
C��1mol����ˮ���ᣨ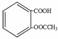 �������Ժ�3molNaOH��Ӧ
�������Ժ�3molNaOH��Ӧ
D���ڼ����ӣ�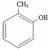 �����Ժ�HCHO�������۷�Ӧ
�����Ժ�HCHO�������۷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA���������ӵ�������ֵ������������ȷ���ǣ�������
| �� | A�� | 1.00 mol•L��1 NaCl��Һ�к���Na+����ĿΪNA |
| �� | B�� | ���³�ѹ�£�6.4 g�������ͳ�����ɵĻ�����к��еķ�������Ϊ0.2NA |
| �� | C�� | ��״���£�1.12 L HCHO��Cԭ�ӵ���ĿΪ0.05 NA |
| �� | D�� | �ڴ��������£�6.4g SO2������������Ӧ����SO3��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������մɡ����ӡ�����ҽҩ�ȷ����й㷺����;������ͨ��������茶����ȷֽ�õ����Ʊ�������茶����ʵ���������£�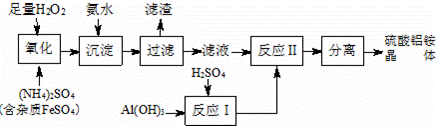
��1��H2O2����FeSO4�����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O����
��2�����백ˮ��Ŀ���ǡ�Fe3+ʹת��ΪFe��OH��3�����仯ѧ��Ӧ����ʽΪ��Fe2��SO4��3+6NH3•H2O=2Fe��OH��3��+3��NH4��2SO4����
��3����Ҫ��֤��Ʒ�Ĵ��ȣ����������백ˮ�������Ƿ��������ʵ������ǣ����Թ�ȡ����ϴ��Һ�����Ӽ���KSCN��Һ������Һ�����ɫ������˵��������ϴ����
��4�����������У������롱�������IJ�������Ϊ��������Ũ����������ȴ�ᾧ�������ˡ�ϴ�ӡ���������������茶�����·ֽ�Ļ�ѧ
����ʽ��2Al2��NH4��2��SO4��4•24H2O ��2��Al2O3+��4��NH3��+��8��SO3��+��26H2O����
��2��Al2O3+��4��NH3��+��8��SO3��+��26H2O����
��5��ȡ4.53g ������茶�����ȷֽ⣬����ʣ��0.51g Al2O3���壮���ȹ����У������������¶ȵı仯��ͼ��ʾ�������ȷ��400��ʱ�������δ�ֽ⣩ʣ�����ɷֵĻ�ѧʽΪ����NH4��2Al2��SO4��4•H2O��������д��������̣���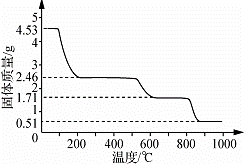
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
.��������(NF3)��һ�����͵��Ӳ��ϣ����ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ�����:HF��NO��HNO3�������й�˵����ȷ����
A.��Ӧ��NF3����������H2O�ǻ�ԭ��
B.��Ӧ�б������뱻��ԭ��ԭ�����ʵ���֮��Ϊ2:1
C.����Ӧ������0.2 mol HNO3����Ӧ��ת��0.2 mol e-
D. NF3�ڳ�ʪ������й©���������������ɫ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���Һ�������������ֳɷ֣������÷�Һ©���������(����)
A���ױ�����֬ B���������������
C�����ͺ�ˮ D�����ͺ����Ȼ�̼
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com