
| A. | 从溴水中萃取溴,可用酒精做萃取剂 | |
| B. | 蒸发实验完毕后,发现蒸发皿炸裂,这是因为没有垫石棉网 | |
| C. | 萃取碘水溶液中碘,分离碘四氯化碳溶液时,眼睛注视分液漏斗里液面 | |
| D. | 蒸馏时,为了加快水的流速,水应从上口进入,下口流出 |
分析 A.萃取剂不能和原溶剂互溶;
B.蒸发皿是可以直接加热的仪器;
C.萃取后分液时,上层液体从上口倒出,下层液体从下口倒出;
D.蒸馏时,冷凝管中的水采用逆流方式.
解答 解:A.萃取剂不能和原溶剂互溶,乙醇和水互溶,所以不能用酒精作溴水的萃取剂,应该用苯或四氯化碳,故A错误;
B.蒸发皿是可以直接加热的仪器,蒸发实验完毕后,发现蒸发皿炸裂,可能是蒸发皿外面有水导致的,故B错误;
C.萃取后分液时,上层液体从上口倒出,下层液体从下口倒出,否则易引进杂质,所以眼睛注视分液漏斗里液面,故C正确;
D.蒸馏时,冷凝管中的水采用逆流方式,水应该从下口进上口出,否则蒸气急剧冷却易炸裂冷凝管,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及萃取的选取、实验操作等知识点,侧重考查学生实验操作能力、实验评价能力,明确实验原理及实验操作规范性是解本题关键,知道萃取剂的选取方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤⑦ | C. | ④⑧ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,推断溶液中含有NH4+ | |
| B. | 无色试液在焰色反应中呈黄色,推断试液是钠盐溶液,不含钾盐 | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,推断溶液中含有CO32- | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,推断溶液中含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入银氨溶液,并水浴加热 | |
| B. | 加入2~3滴石蕊试液 | |
| C. | 先加入浓NaOH溶液,加热蒸馏,把蒸馏出的物质加银氨溶液并水浴加热 | |
| D. | 直接蒸馏,把蒸馏出的物质加NaOH溶液调至碱性,再加银氨溶液,并水浴加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
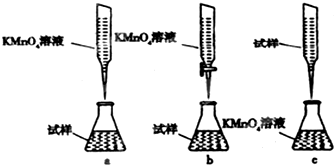
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
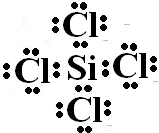 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质A的转化率小了 | B. | 平衡向正反应方向移动了 | ||
| C. | 物质B的质量分数减小了 | D. | b>a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com