
| A. | 某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,该溶液中一定含有CO32- | |
| B. | 除去HNO3溶液中的少量H2SO4,可加适量BaCl2溶液 | |
| C. | 利用焰色反应可以将NaCl和KCl两种无色溶液鉴别出来 | |
| D. | 某溶液中滴加烧碱溶液,加热产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定存在NH4+ |
分析 A.无色气体为二氧化碳或二氧化硫;
B.硫酸与氯化钡反应生成硫酸钡沉淀和HCl;
C.焰色反应分别为黄色、紫色;
D.使湿润的红色石蕊试纸变蓝的气体为氨气.
解答 解:A.无色气体为二氧化碳或二氧化硫,则将气体通入澄清石灰水中,溶液变浑浊,该溶液中可能含有CO32-或HCO3-,或SO32-等,故A错误;
B.硫酸与氯化钡反应生成硫酸钡沉淀和HCl,引入新杂质,不能除杂,故B错误;
C.焰色反应分别为黄色、紫色,现象不同,可鉴别,故C正确;
D.使湿润的红色石蕊试纸变蓝的气体为氨气,则原溶液中一定存在NH4+,故D正确;
故选CD.
点评 本题考查化学实验方案的评价,为高频考点,涉及常见离子的检验、混合物分离提纯等,把握物质的性质、性质差异及混合物分离提纯为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
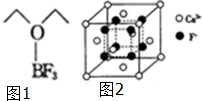 氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
氟及氟产品在工农业生产中应用非常广泛,回答下列问题: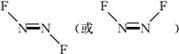 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HF>HCl>HBr>HI | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 离子半径:N3->O2->F->Na+>Mg2+ | D. | 沸点:F2>Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 的说法正确的是( )
的说法正确的是( )| A. | 该物质为丁烷 | B. | 该物质的分子式为C4H8 | ||
| C. | 该物质为丁烯 | D. | 该物质化学性质与苯相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2CO3固体 | B. | 水 | C. | CaCO3固体 | D. | NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
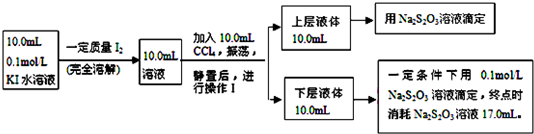
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
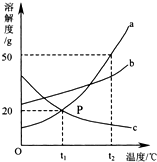 如图是A、B、C三种固体物质的溶解度曲线图,请回答:
如图是A、B、C三种固体物质的溶解度曲线图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com