
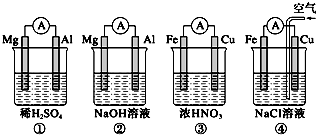
| A、①②中Mg作负极,③④中Fe作负极 |
| B、②中Mg作正极,电极反应式为6H2O+6e-═6OH-+3H2↑ |
| C、③中Cu作负极,电极反应式为Cu-2e-═Cu2+ |
| D、④中Cu作正极,电极反应式为2H++2e-═H2↑ |


科目:高中化学 来源: 题型:
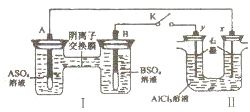 某同学按如图所示的装置进行试验.A、B两种常见金属,它们的硫酸盐可溶于水,当K闭合时,在交换膜处SO42-从右向左移动.下列说法错误的是( )
某同学按如图所示的装置进行试验.A、B两种常见金属,它们的硫酸盐可溶于水,当K闭合时,在交换膜处SO42-从右向左移动.下列说法错误的是( )| A、电解一段时间后,向Ⅱ装置通入适量的HCl气体可以恢复原来的浓度 |
| B、反应初期,y电极周围出现白色沉淀 |
| C、B电极质量增加 |
| D、x电极产生气泡,且生成1mol气体的同时,有1molA参与反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
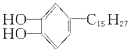 是生漆的主要成分,黄色,能溶于有机溶剂中,生漆涂在物体表面,能在空气中干燥转变为黑色漆膜,它不具有的化学性质为( )
是生漆的主要成分,黄色,能溶于有机溶剂中,生漆涂在物体表面,能在空气中干燥转变为黑色漆膜,它不具有的化学性质为( )| A、可以燃烧,当氧气充分时,产物为CO2和H2O |
| B、与FeCl3溶液发生显色反应 |
| C、能发生取代反应和加成反应 |
| D、能溶于水、酒精和乙醚中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、HI>HCl>NH3 |
| B、HCl>NH3>HI |
| C、HCl>HI>NH3 |
| D、NH3>HI>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:3 |
| C、3:2 | D、任意比 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2+、Fe3+ |
| B、Fe2+、Cu2+ |
| C、Fe3+、Cu2+ |
| D、Cu+、Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com